Volver a ¨Psicofarmacología – Psicodinámica IV (Indice General)¨
1-1. Conceptos del tratamiento psicofarmacológico
– Psicofarmacoterapia
La invasión cuantitativa (psicológica y neuroquímica) desorganiza el aparato psíquico, siendo necesario la administración de psicofármacos para restablecer el orden de la cualidad y las representaciones.
En un proceso psicoterapéutico se indica una medicación psicofarmacológica como último recurso. El psicoterapeuta «se desentiende» del azar y avatar de quien la administra y de quien la recibe, y trata de no involucrarse y conservar una falsa asepsia psicoterapéutica.
De la misma manera que la medicina «se desentendió» de la psiquiatría y de la psicología durante siglos, hoy se corre el peligro inverso: que ambas disciplinas hagan caso omiso de conceptos médicos de investigación y tratamiento, y recurran de forma unilateral a la curación por la palabra, sin evaluar que muchas veces con ella no basta.
La Real Academia Española de la Lengua define a la psiquiatría como la doctrina de las enfermedades mentales y su tratamiento, y a la psicología como la ciencia que se ocupa de los fenómenos psíquicos, de la vida subjetiva, de su medición y de cuantas relaciones entre los aspectos psíquicos y físicos puedan establecerse (sentimientos, ideas, emociones, reacciones, tendencias electivas, instintos, etc.) .
Pese a estas definiciones, la psiquiatría trató de ajustarse a un modelo médico clásico, a la espera de que, con los nuevos descubrimientos (al igual que la microbiología o la patología, por ejemplo) la considerasen como un par más dentro de la familia de las ciencias médicas. Esta lucha infructuosa comenzó con la aceptación de dos falsos postulados.
El primero fue no querer reconocer que, por definición, la psiquiatría y la psicología investigan fenómenos que el ser humano genera a través de su aparato psíquico. El segundo fue creer que el modelo médico cumple rigurosamente con los cuatro postulados clásicos, por el cual se afirma la existencia de una enfermedad:
1. Posee etiología específica.
2. Existe una discontinuidad con la normalidad. 3. Presenta cambios físicos demostrables.
4. Comenzada la noxa interna, ésta no es modificable por influencias ambientales externas.
Sin embargo, la realidad indica diferencias:
1. Aun el bacilo de Koch (etiología específica de la tuberculosis) necesita de factores personales del huésped (hiponutrición) y del medio ambiente externo para desencadenar la enfermedad (condiciones deficitarias del hábitat).
2. No es posible delimitar tan claramente la discontinuidad o corte entre lo normal y lo anormal. Ni aun en la clínica médica los valores altos momentáneos de presión arterial o la acidez gástrica esporádica pueden indicar la existencia de la enfermedad hipertensiva o ulcerosa.
En cambio, en la actualidad se reconoce que factores emocionales pueden provocar el aumento de la cantidad de neurotransmisores cerebrales (de noradrenalina, en el caso de la hipertensión, o de acetilcolina, en el caso de la acidez), sin poder afirmar que ello significa una clara patología orgánica.
3. En las epilepsias o en las arritmias no hay cambios físicos demostrables.
4. Los traumas y las noxas internas pueden ser modificables por el medio externo, ya que los sistemas defensivos inmunitarios también dependen de factores emocionales (las enfermedades de autoagresión no reconocen sus antígenos como propios y generan anticuerpos en su contra).
Desde la perspectiva del tratamiento, la psicoterapia tiene sus antecedentes en el «tratamiento moral» de Pinel, quien liberó a los enfermos mentales de las prisiones y del encadenamiento a que estaban sometidos.
Pero es recién con Freud que se comienza a utilizar el «tratamiento del alma» en forma científica.
Desde su Proyecto para neurólogos», Freud enfatiza el concepto de una magnitud de excitación que se desplaza a lo largo de cadenas neuronales. Su descripción económica unida a la orientación tópica y dinámica estructurarán, más tarde, la metapsicología.
La hipótesis de un aparato (neuronal, en el Proyecto»; psíquico, en La interpretación de los sueños) que tiende a mantener lo más bajo posible su nivel de energía, permite a Freud describir el «principio de constancia» (26).
En la medida en que el aparato recibe excitaciones de origen externo e interno se halla sometido a una exigencia de trabajo, que implica el pasaje de la cantidad a la cualidad, es decir, una tendencia permanente a liberarse de excedentes de tensión. Se cumple aquí el «principio de constancia».
El paradigma de la invasión cuantitativa es el trauma. Dice Freud (comunicación preliminar a ‘Introducción al psicoanálisis»),
[ … ] «lo utilizamos para designar aquellos sucesos que, aportando a la vida psíquica en brevísimos instantes un enorme incremento de energía, hacen imposible la su presión o asimilación de la misma por los medios normales y provocan, de este modo, duraderas perturbaciones del aprovechamiento de la energía…
Es necesario agregar a la invasión cuantitativa la incapacidad del sujeto de responder a ella adecuadamente.
Esta adecuación se halla vinculada a la capacidad de controlar y elaborar psíquicamente esa excitación. No debemos olvidar que es en los primeros momentos de la vida cuando esta incapacidad es más evidente, dado que el aparato psíquico aún no está estructurado.
En el trauma falla el «principio de constancia», ya que el aparato es incapaz de descargar la excitación a través de ligaduras psíquicas.
Obviamente, Freud nunca abandonó su teoría traumática. Se puede ver que, en trabajos muy posteriores, se refiere a ella. Es allí donde plantea que un aflujo excesivo de excitación anula inmediatamente el principio de placer, obligando al aparato psíquico a realizar una tarea más urgente: ligar las excitaciones para posibilitar su descarga ulterior. Para poder actuar, el principio de placer necesita que se cumplan ciertas condiciones, que son anuladas por el traumatismo.
En Inhibición, síntoma y angustia, el yo, al desencadenar la señal de angustia, trata de no verse desbordado por la angustia automática, que caracteriza a la situación traumática.
En 1938, cuando se descubren las primeras hormonas, Freud se anticipa al futuro de poder actuar químicamente sobre el aparato psíquico cuando afirma en «Esquema del Psicoanálisis»:
[ … ] pero la terapia nos ocupa aquí únicamente en la medida en que ella trabaja con medios psicológicos. Quizás el futuro nos enseñe a influir en forma directa, por medio de sustancias químicas específicas, sobre los volúmenes de energía y sus distribuciones dentro del aparato anímico. Puede ser que se abran para la terapia otras insospechadas posibilidades: por ahora no poseemos nada mejor que la técnica psicoanalítica, razón por la cual no se debería despreciarla a pesar de sus limitaciones.
A partir de 1950, con la aparición de los primeros psicofármacos, es cuando la psicofarmacología progresa de forma vertiginosa, aprovechando el avance de otras ciencias biológicas, ya que puede sintetizar fármacos de influencia cada vez mayor sobre el aparato psíquico.
La psiquiatría deja de ser una ciencia estática al nutrirse del psicoanálisis (mayor comprensión de los conflictos intrapsíquicos) y de la psicofarmacoterapia (aceptación de la acción farmacológica dentro del proceso psicoterapéutico)
Hoy se conoce que la sinapsis está gobernada por los neurotransmisores, que permiten a las células nerviosas entrar en contacto unas con otras, conservar su individualidad y dejar ese espacio intersináptico como sistema de comunicación y de transmisión de la información.
En la actualidad existen métodos para investigar la estructura nerviosa central (resonancia magnética nuclear, tomografía por emisión de positrones), la neuroquímica cerebral (dosaje de neurotransmisores) y la bioelectricidad (mapeo cerebral computarizado).
Se conoce que la esquizofrenia y la enfermedad maníaco-depresiva pueden ser exacerbadas o atenuadas por sustancias químicas endógenas (dimetiltriptamina, sustancias similbenzodiazepínicas, metoxifenfiglicol) o exógenas (sustancias adictivas, medicamentos).
También existen pruebas de la existencia de ciertas relaciones genéticas en la esquizofrenia, en la enfermedad maníaco-depresiva y en los enfermos suicidas, sociópatas y alcohólicos.
Kraepelin dividió las psicosis funcionales (las que para aquella época no tenían alteraciones estructurales) en maníaco-depresivas y esquizofrenias. Las primeras, con un trastorno del ánimo o humor con recuperación completa luego del episodio agudo, y las segundas, en las que luego de la remisión de los síntomas aparecía un deterioro emocional-social con pérdida de interés e iniciativa.
Hoy se puede demostrar que las esquizofrenias con síntomas «negativos» (abulia, indiferencia afectivo-social, etc.) corresponden a un tipo -el llamado por Crow esquizofrenia de tipo II u orgánica-, con alteraciones estructurales en la resonancia magnética nuclear y en la tomografía positrónica.
Estos adelantos permiten integrar la psiquiatría descriptiva fenoménica y la psiquiatría dinámica o psicoanalítica. La primera permitió unificar síntomas y establecer acuerdos en la terminología de las enfermedades mentales, dando lugar a clasificaciones sintomáticas que beneficiaron el uso racional de los psicofármacos.
En cambio, la psiquiatría con apuntalamiento psicoanalítico nos advierte acerca del peligro de las generalizaciones clasificatorias apresuradas y nos invita a considerar a cada ser humano como único e irrepetible. Es necesario tener en cuenta ambas vertientes y reconsiderar las dificultades que puede ocasionar el enrolarse exageradamente en una u otra postura.
La psiquiatría psicoanalítica reconoce la existencia de un sistema inconsciente y trabaja con los conflictos entre las diferentes instancias.
El psicofármaco puede aquí considerarse como un objeto que suele actuar cuando la palabra (orden de la cualidad y de las representaciones) desaparece como consecuencia de la invasión cuantitativa del aparato. La psicosis comporta un ataque de esta naturaleza, cantidad que no pudo ser cualificada oportunamente.
Si tomamos la experiencia de satisfacción (modelo de constitución del aparato psíquico, en La interpretación de los sueños) como modelo de transformación de cantidad en cualidad, se puede ver que en la medida en que este cambio no es posible, el aparato se conforma fallidamente.
Por lo tanto, siempre estaría al acecho un ataque masivo cuantitativo que el psicótico tratará de cualificar a través de sus mecanismos restitutivos. Esta invasión de excitación genera patología en la medida en que desarticula y desorganiza la lábil configuración yoica. Es ahí donde el trauma (enorme incremento de energía) sigue teniendo vigencia.
En la neurosis, la idea de conflicto nos remite a la presencia cualitativa. La represión primaria ha constituido un aparato psíquico. Las representaciones reprimidas buscarán un camino sustitutivo y se generarán formaciones de compromiso (síntomas, sueños).
Si el yo se separa de uno de sus principales órganos constitutivos, como es el juicio de realidad, y toma partido por el ello, se desencadenará la psicosis. Si lo hace por el mundo exterior, la neurosis, y si se sobreadapta dará lugar a las enfermedades psicosomáticas.
La desestructuración-desintegración, debido a esa gran invasión de energía al aparato psíquico, puede ser parcial (neurosis) o total (psicosis).
En el primer caso, un intenso acceso de ansiedad o una crisis de pánico muestran la caída momentánea del nivel representacional; en el segundo, un brote esquizofrénico indica la pérdida total de la lábil construcción restitutiva, que permitía al paciente «vivir» hasta ese momento.
Al no ser posible contener desde el yo e integrar estas cargas para todo el self, es cuando se agota la palabra y se hace necesario recurrir a los psicofármacos, ya sea para disminuir la excitación (en caso de psicofármacos antipsicóticos) o de aumentarla (en caso de depresiones con psicofármacos antidepresivos). En este último caso, la no fusión pulsional y por lo tanto el predominio de la pulsión de muerte provocan que la pura cantidad se aloje a nivel de una instancia: el ideal del yo que tortura y somete al yo.
También se deberá tener en cuenta la utilidad de los psicofármacos en las fases profilácticas. Conflictos muy dolorosos o regresivos del orden vital (separaciones, duelos, pérdidas laborales, etc.) pueden dar lugar a respuestas cuantitativas (que en general la familia y el terapeuta conocen) y que es recomendable prevenir con la administración profiláctica de psicofármacos, para no provocar situaciones de «brotes», recaídas o accesos de mayor gravedad.
La compliance es la relación médico-paciente farmacoterapéutica, en la que el paciente toma la medicación según la directiva médica. Ésta puede ser con la clásica actitud paternalista de la «autoridad médica» o a través de la «alianza terapéutica».
Es conveniente buscar la forma de evitar las actitudes mágicas referentes a los medicamentos, ya que las drogas o hierbas, cuya acción farmacológica no puede ser demostrada, cuentan, desde un comienzo, con una alianza paciente-terapeuta del «principio mágico de la curación».
Se tratará, así, de establecer una sólida base, con alianza científica, que permita evitar caer en relaciones transferenciales de idolatría o de hechicería si se tiene éxito, o denigratorias, si se fracasa.
Hablamos al principio de un «desentendimiento» por parte del psicoterapeuta referido a no involucrarse con el tema de la medicación psicofarmacológica. Más allá de la asepsia psicoterapéutica es necesario evaluar las implicancias contratransferenciales de las invasiones cuantitativas. En la medida en que estos aspectos se puedan tener en cuenta, los abordajes psicoterapéutico y psicofarmacológico podrían aunarse para el logro del objetivo común a ambos,
Se puede definir la psicofarmacología como la rama de la farmacología que estudia los efectos de sustancias químicas sobre el psiquismo normal o patológico, sin restringirse al estudio de sustancias de efectos beneficiosos para los enfermos, sino incluyendo todas aquellas que lo modifican en sentido favorable o desfavorable.
El efecto obtenido podrá variar no solamente por las características propias del psicofármaco (factores específicos) sino además por las diferentes expectativas que se depositan en el medicamento (factores inespecíficos) .
1-2. Factores inespecíficos del tratamiento psicofarmacológico
Los psicofármacos producen acciones sobre los receptores sinápticos, que no dependen de la farmacología clásica, ya que, a diferencia de otros medicamentos, están influidos por factores emocionales, afectivos y comporta mentales que originan señales que actúan sobre el mismo receptor.
Se denomina de este modo a todos aquellos efectos que no dependen de las propiedades farmacológicas de la sustancia psicotrópica y pueden modificar la respuesta terapéutica. Estos efectos variables darán una resultante que, juntamente con los factores específicos, producirá determinados efectos sobre la sintomatología de forma positiva, negativa o indistinta. Entre estos factores se cuentan las expectativas acerca del efecto del psicofármaco administrado.
Las expectativas ante la medicación provienen tanto del paciente como del médico que administra el psicofármaco, el psicoterapeuta que lo indicó, los familiares y el ámbito sociocultural en el cual se desenvuelve el enfermo.
El paciente espera de la medicación que recibe la reducción o supresión de los síntomas, que son para él la causa de su sufrimiento psíquico. Será posible obtener buena respuesta a la psicofarmacoterapia si el enfermo tiene conciencia de lo que le ocurre, desea ser tratado, reacciona positivamente al tratamiento psíquico efectuado y tiene una buena opinión de los profesionales intervinientes. Por el contrario, la respuesta al tratamiento será dudosa o mala si considera que sus trastornos están más relacionados con la esfera somática que con la psíquica, si sus expectativas frente a la medicación administrada son desmedidas o ha tenido una mala experiencia con tratamientos anteriores.
El médico que tiene a su cargo la administración del psicofármaco, por su parte, espera controlar los síntomas que considera patológicos (target symptoms).
En este punto, las posibilidades de obtener éxito serán mayores cuando el profesional asuma una actitud comprensiva y sensible. Los límites de permisividad o prohibición deben ser claros, para que no generen conflictos con el enfermo y su familia. Esto último se torna imprescindible con enfermos psicóticos, en cuyo caso la medicación deberá ser administrada por un familiar.
Por el contrario, la respuesta será dudosa o mala si el médico es poco sensible, carece de la necesaria autoridad, cree más en el tratamiento psicológico o tiene un mal pronóstico del paciente.
Por otra parte, los efectos psicofarmacológicos pueden ser negativos si el enfermo no está controlado psicológicamente y no existe un lugar donde su «palabra» pueda ser tratada.
La necesidad de un médico responsable del control psicofarmacológico se fue imponiendo debido al avance científico y técnico.
La ventaja del terapeuta como médico administrador reside en que detecta con mayor precocidad los pequeños cambios al observar y escuchar de modo más frecuente al paciente, lo que le permite efectuar cambios de dosificación y medicamentos de forma rápida.
La desventaja para el paciente es que deja de tener un lugar médico convencional para autoevaluarse, y para el psicoterapeuta, es que deberá aceptar el estudio de una nueva disciplina que cambia continuamente y que requiere una permanente actualización.
La ventaja del tratamiento al existir un médico administrador es que el paciente no podrá utilizar los síntomas psicopatológicos como mecanismos de defensa, ya que la evaluación de la mejoría se basará en la mejoría (o no) de los síntomas después del tratamiento psicofarmacológico y en la aparición de efectos adversos. La desventaja es que aumenta la distancia transferencial.
Las expectativas familiares, especialmente en el caso de pacientes psicóticos o con déficit mental, son quizá las más difíciles de satisfacer. Más que de expectativas, la mayoría de las veces se trata de exigencias, no solamente respecto de la medicación sino también hacia los profesionales tratantes. Es necesario aclarar y definir los límites de la actuación que corresponde a cada uno de los profesionales intervinientes, como también de la que corresponde a los familiares que se hagan cargo de comprar, guardar y administrar los psicofármacos recetados.
Las expectativas socioculturales varían en nuestro medio desde las de quienes confían en que se logrará la resocialización de los enfermos mediante psicofármacos, hasta las de quienes argumentan que el «chaleco psicofarmacológico» no difiere sustancialmente de los chalecos de fuerza usados en épocas pasadas en los hospicios.
Por otra parte, la presión que en una sociedad difícil y compleja se ejerce sobre el individuo, de quien se espera que manifieste un equilibrio psíquico «adulto y responsable», resulta muchas veces un factor de desequilibrio que desemboca en síntomas neuróticos, psicosomáticos y aun psicóticos.
De esta forma, la automedicación o la exigencia de medicación psicofarmacológica al médico de cabecera se constituyen en psicoterapias de urgencia.
El incremento del consumo de psicofármacos se debe a la aspiración de encontrar la «pastilla salvadora», que pueda yugular rápidamente las angustias y depresiones sin entrar a analizar de forma profunda los diferentes conflictos psicopatológicos de la estructura individual y, finalmente, de la sociedad.
Muchas veces, el papel salvador que se asigna al medicamento se origina en una expectativa familiar que se transmite sucesivamente al enfermo, al psicoterapeuta, al médico y, finalmente, a quien administra la medicación.
La falacia de este «poder mágico de curación», idealizado por la familia, se pone de manifiesto fácilmente cuando se intenta utilizar el psicofármaco como único elemento para eliminar síntomas molestos o que desagradan en el ambiente socio-familiar del enfermo. De esta forma se pretende dar a la psicofarmacología un peso mayor que a los demás tratamientos dinámicos de la psiquiatría actual (psicoterapia individual, familiar, grupal, laborterapia, musicoterapia, expresión corporal, etc.).
De no tenerse en cuenta estos elementos, se cierra un círculo vicioso por demás nocivo que resulta imposible contrarrestar.
Las diversas sensaciones que afluyen y desorganizan al enfermo psicótico y que lo van alejando de la realidad hacen imprescindible la inclusión del psicofármaco para tratar de disminuir esta invasión desorganizante y volver a la situación anterior (medicamentos antipsicóticos). Este proceso se produce también en las neurosis, claro está que no con la misma magnitud. La ayuda que brinda el psicofármaco corre peligro de desaparecer cuando se pretende asignarle la responsabilidad de un cambio de calidad, cambio que está, casi en forma exclusiva, reservado a la psicoterapia.
Un factor inespecífico importante es el prospecto de envase que acompaña al medicamento. Al igual que sus colegas de otras ramas de la medicina, los médicos que atienden a esta clase de pacientes no suelen aclararles el contenido del prospecto. Una razón es el «sentimiento de omnipotencia médica», la creencia de que lo dicho por el profesional será aceptado y seguido sin reparos por el enfermo. También sucede que el médico rara vez tiene entre sus manos el envase original del medicamento que el paciente adquiere en la farmacia. Desconoce así color, forma, tamaño y tipo del envase que contiene el medicamento por él recetado. Generalmente ignora lo que la empresa farmacéutica ha impreso en el prospecto de envase, en cumplimiento de las normas dictadas por el Ministerio de Salud Pública. Así, el enfermo se encuentra, por un lado, con una receta que indica en qué momentos del día deberá tomar su medicamento, que según lo que le dijo el médico aliviará sus síntomas y, por el otro, con un prospecto que no indica para qué sirve ese medicamento pero sí cuáles son sus contraindicaciones y los efectos adversos que puede llegar a producir.
O sea que esta información, que debería ser complementaria, se transforma en antagónica para el paciente, quien la interpretará de acuerdo con su personalidad.
Los efectos colaterales o adversos se presentan sólo en un determinado porcentaje de casos, pero el paciente no lo ve así. Su expectativa es entonces que éstos aparecerán inevitablemente cuando comience a tomar el psicofármaco recetado.
El médico puede obviar este inconveniente aclarando al paciente que conoce del psicofármaco no sólo sus posibles beneficios sino también los trastornos que puede provocar. Dará seguridad al paciente si le indica que de presentarse algún efecto no deseado no hesite en comunicárselo, ya que, por ejemplo, la sequedad de boca molesta, provocada por la administración de antidepresivos, puede fácilmente superarse masticando chicles para aumentar la secreción salival, o si este síntoma es tolerable, esperando un par de días hasta que desaparezca, al adaptarse a la nueva situación los mecanismos compensatorios del organismo.
Muchas veces la medicación psicofarmacológica es prescrita por el médico general que asiste al paciente por patologías de origen «somático». Por lo común esto ocurre cuando la historia clínica revela síntomas fundamentalmente ansiosos y/o depresivos. Ya está lejana la discusión entre quienes consideraban incompatible la medicación, que provoca alivio sintomático, con el tratamiento psicoanalítico, que al identificar las causas profundas de la enfermedad produce alivio curativo. En los últimos años se han llegado a comprender mejor las interacciones entre psicoterapia y psicofarmacología. Planteados los métodos psicoterapéuticos como un diálogo verbal entre paciente y terapeuta, cuyo objetivo es obtener una modificación con alivio de un sufrimiento psíquico, es conveniente que quien administra la medicación esté fuera de ese ámbito «verbal». De esa manera se consigue un efecto positivo de la medicación sobre la psicoterapia al tener el paciente otro lugar con un encuadre de consulta médica habitual, donde puede hablar de síntomas psíquicos o somáticos como ansiedad, insomnio, pérdida de memoria, constipación, cte., sin sentirse molesto («perseguido») por la interpretación psicopatológica de esos síntomas.
La prescripción de un psicofármaco no se aparta de la norma general médica de recetar medicamentos como corolario de un examen clínico y un diagnóstico presuntivo. No es de interés puntualizar en este libro la metodología de la entrevista psiquiátrica. Pero se deben, dado lo específico de este tipo de consultas, señalar algunos antecedentes y motivos actuales de enfermedad. Por lo general, el paciente manifiesta en la consulta que «le recomendaron tomar algo para los nervios» (indicación hecha por otro profesional, por la familia, por los amigos, cte.). Se podrían distinguir cinco grandes áreas:
a) el cuerpo,
b) la afectividad,
c) el pensamiento,
d) la memoria, y
e) los hábitos orales infantiles.
Cada una de estas áreas deberá ser investigada cuidadosamente, en relación con el presente y el pasado; aun cuando ello requiera más de una entrevista, el tiempo así empleado redundará en beneficio de un plan de tratamiento efectivo.
En los trastornos en el área del cuerpo (dolores, taquicardia, etc.) se deberá prestar especial atención a ansiedades y depresiones y a sus factores desencadenantes.
En el trastorno afectivo melancólico se deberá interrogar a fondo al paciente, ya que la historia de sus antecedentes nos mostrará si hubo algún episodio o episodios con intentos de suicidio o fantasía, ideas suicidas o equivalentes (accidentes, descuidos, cte.); duelos que han sido reprimidos y han quedado enquistados y se reactivan ante situaciones similares (depresión neurótica), etcétera.
Las alteraciones del pensamiento orientarán hacia una ruptura con la realidad y el mundo exterior y a diferentes tipos de ideación patológica que pueden determinar un diagnóstico de condición fronteriza, núcleos psicóticos graves o psicosis.
Las alteraciones de la memoria por sí solas, o juntamente con otros síntomas, requieren que se investigue una posible «organicidad» (arteriosclerosis, epilepsia, demencia, etc.).
Los hábitos orales infantiles (cafeinismo, tabaquismo, etc.) señalan, en una primera apreciación, la necesidad oral como sustituto de carencias afectivas muy primarias.
En el período agudo el objetivo es:
a) disminuir el nivel de excitación, cuando éste impide al paciente pensar y reflexionar sobre estos conflictos (antipsicóticos y tranquilizantes);
b) aumentar el nivel de excitación para reactivar sus posibilidades de control sobre su estado inhibido o depresivo (antidepresivos).
En la fase crónica o profiláctica el objetivo es:
c) tratar de impedir respuestas cuantitativas que el psicoterapeuta, por su conocimiento del enfermo, puede anticipar y desea prevenir. 0, por el contrario, en el caso de conflictos muy dolorosos y regresivos que puedan dar lugar a respuestas difíciles de prever (antipsicóticos, tranquilizantes, antidepresivos y/o psicoestimulantes);
d) impedir una invasión desorganizante, que provoque la pérdida del juicio de realidad (psicosis) (antipsicóticos).
Aun en enfermos crónicos, deteriorados y confusos, que han sido tratados con los psicofármacos más eficaces, no deben obviarse los pasos descritos. De no poderse dialogar con el enfermo, la reunión familiar con la mayor cantidad de integrantes que tuvieron o tienen vinculación con el enfermo aporta datos muchas veces sorprendentes. Así, por ejemplo, en el caso de un geronte confuso y que no controlaba los esfínteres, se comprobó que ello ocurría porque el personal de servicio de la casa, cumpliendo una indicación dada por un médico años antes, le administraba un neuroléptico que en esas dosis actuaba como hipnótico. En estos casos basta con hacer un plan coherente y global de tratamiento junto con el psicoterapeuta y el médico general para conseguir una resocialización adecuada. Aun en esquizofrenias crónicas residuales, las medidas complementarias de recreación, j unto con un tratamiento con neurolépticos, pueden tener efectos terapéuticos insospechados.
Antes de instrumentar la medicación es, pues, imprescindible realizar una correcta historia clínica psicofarmacológica que abarque:
– Motivo de consulta y derivación.
– Medicación actual.
– Motivo de prescripciones anteriores.
– Afecciones somáticas.
– Hábitos orales y necesidad de psicoestimulación (café, colas, tabaco, alcohol).
– Sociabilidad y comentarios acerca de la medicación que suele tomar.
– Motivo, esquema y seguimiento de la prescripción actual.
Es importante recabar datos de medicaciones anteriores. Así, por ejemplo, en un paciente depresivo actual, el haber usado anfetaminas o cocaína en épocas estudiantiles para psicoestimularse orientará la terapéutica al uso de antidepresivos desinhibidores. La sensibilidad extrapiramidal a fármacos neurolépticos indicará el uso de antiparkinsonianos profilácticos.
El seguimiento del enfermo debe hacerse con una determinada frecuencia, ya sea de forma personal o telefónica; en casos graves o difíciles de evaluar, se deberán recabar los datos evolutivos de la medicación al familiar o garante de la administración medicamentosa. La valoración semiológica adecuada del paciente debe diferenciarse de «equivalentes transferenciales» (fenómeno placebo: respuesta positiva o negativa antes que la respuesta farmacocinética esperada tenga lugar) y de «equivalentes contratransferenciales» (1os cambios negativos o positivos que hace el paciente son intolerables para el equipo psicoterapéutico» o «los impulsos del paciente son peligrosos si no están controlados por los psicofármacos»).
Finalmente, la mejoría no indica un alta absoluta ya que la medicación, al no ser curativa, origina, tanto en el paciente como en el terapeuta, fantasías de recidivas o recaídas en la enfermedad.
1-3. Factores específicos del tratamiento psicofarmacológico: Conceptos de farmacología y de neurobiología molecular
Los psicofármacos actúan por mecanismos farmacológicos y moleculares de corto y largo plazo, a través de la modificación de neurotransmisores y de mensajeros citoplasmáticos y nucleares celulares, respectivamente.
Los factores específicos más importantes en la administración de psicofármacos son los que corresponden a la farmacodinamia, la farmacocinética y la biodisponibilidad, desde el punto de vista de la farmacología clásica y aquellos nuevos conceptos desarrollados desde la biología molecular como son el citoesqueleto, la transducción neuroquímica, las biomembranas, la transcripción genética y la neuroplasticidad.
La acción de los psicofármacos sobre los neurotransmisores ha dejado de ser la única responsable de los cambios, que a nivel cerebral, originarán los cambios conductales esperados. Se puede afirmar en la actualidad, que las acciones lentas y a largo plazo, serán las mediadoras de dichos cambios, ya que una vez suspendida la medicación, los mismos podrán conservarse, si quedan almacenados en la «memoria neuronal». En realidad los cambios producidos en los cuartos mensajeros (ADN-ANRm intranucleares) serán los encargados de los cambios genéticos.
La información transmitida a través de los cambios en la postsinapsis, como son la activación intracelular de la regulación genética neuronal, mediada por la transcripción a través del ADN-ARN, serán los que provocarán los cambios deseados. Es decir que los psicofármacos, sea por su acción sobre los neurotransmisores o sobre las proteínas, serán los que inducirán los cambios en la neuroplasticidad neuronal (habilidad de la neurona para aprender y adaptarse).
La farmacodinamia es el estudio fisiológico y bioquímico de los efectos que produce el fármaco en los sitios donde actúa.
La farmacocinética es el estudio de los procesos de absorción, distribución, metabolismo y excreción del fármaco. La concentración del psicofármaco a nivel del receptor y su unión reversible o irreversible con éste determinarán la acción de la droga. Es decir, se trata de establecer la relación existente entre las dosis y el tiempo durante el cual se ejerce la acción del fármaco.
La biodisponibilidad es la cantidad de droga que puede ser absorbida y llega a la circulación general. Más que la absorción genérica, lo que tiene importancia es la fracción absorbida durante los intervalos que separan la administración de las dosis. Para un esquema fijo de dosificación, la acumulación irá en aumento si estos intervalos son cortos.
La mayoría de los psicofármacos se absorben pasivamente por difusión. Para difundirse a través de las membranas celulares, los psicofármacos, que a excepción del litio son macromoleculares, deben ser liposolubles. La liposolubilidad depende del pH del psicofármaco y del medio. Así, por ejemplo, los barbitúricos se absorben en el medio ácido del estómago, y los antidepresivos, en el medio alcalino del duodeno.
Procesos gástricos (gastritis), duodenales (úlcera duodenal) o que interfieran con el pH y las características morfológicas de las mucosas impedirán la normal absorción del psicofármaco. En los gerontes la disminución de la circulación intestinal y los procesos celulares involutivos provocan una menor absorción pero también una menor metabolización, dando origen a fenómenos tóxicos si no se reduce la dosis.
También existen psicofármacos como el clordiazepóxido o el diazepam. que se absorben mejor por vía gastrointestinal que por vía intramuscular.
Estados Unidos, 500 mg en Suiza y 300 mg en Inglaterra; en nuestro país, si bien no hay datos estadísticos, es aún mucho más baja. Si este fenómeno se debe o no a factores culturales, está aún por dilucidarse. Sin embargo, aparece de forma clara que en aquellos estudios que brindan a los enfermos psicóticos una contención psicoterapéutica global, el psicofármaco puede ser dosificado de manera notoriamente menor. El beneficio que se logra con este criterio es indiscutible, ya que permite reducir la toxicidad y los efectos secundarios indeseables.
La mayoría de los psicofármacos siguen una cinética de primer orden, lo que significa que la cantidad que se elimina es proporcional a la cantidad de droga que circula en el plasma. Esto permite calcular la vida media (tiempo requerido para que la concentración de una droga disminuya a la mitad). El estado estacionario, es el equilibrio entre la cantidad de droga ingerida y la eliminada, y la concentración plasmática se mantiene constante, El estado estacionario suele alcanzarse luego de seis vidas medias, y a la inversa, cuando se interrumpe un fármaco, se necesitan seis vidas medias para su completa eliminación.
Las interacciones farmaroquinéticas se refieren a la habilidad de una droga en afectar la absorción, la distribución, el metabolismo y la eliminación de otra.
Existen más de 200 tipos de citocromos P450 que se localizan en el retículo endoplásmico del hígado, en intestino delgado y duodeno, permitiendo la eliminación de los psicofármacos.
Los citocromos P450 se clasifican en familias y en subfamilias, que se denominan con la sigla CYP o P450. En primer lugar se coloca un número que representa una familia de aminoácidos con una secuencia similar al 36 %, en segundo lugar de una letra de la subfamilia, que representa una secuencia de aminoácidos similar el 70 % y por último un número que individualiza al gen. Así existen la P450 o CYP IA2; la 2C9/10/19; la 2D6, la 3A3/ 4, etc.
1-4. Mecanismo de acción de los psicofármacos
Los psicofármacos actúan a través de los neurotransmisores en la sinapsis, provocan la hiperpolarización o despolarización celular (inhibición o excitación neuronal).
En el cerebro la transmisión de la información se hace a través de la conducción del impulso nervioso (excitatorio o inhibitorio) por medio de cadenas de neuronas íntimamente relacionadas unas con otras, La «información»o impulso es «captada» por numerosas prolongaciones del cuerpo celular de la neurona llamadas dendritas, que de esta forma aumentan notoriamente la superficie receptiva. La neurona emite o «dispara» el impulso nervioso a través de una prolongación generalmente única llamada axón, que termina en una pequeña expansión en forma de bulbo, denominada botón terminal.
Los fármacos deben actuar sobre los elementos citoplasmáticos y nucleares de las células elegidas («células target o blanco»), para, a través de sistemas enzimáticos (o «mensajeros») intracelulares, puedan llegar al núcleo y modificar la actividad génica. Esta forma en que un estímulo externo induce una respuesta de las neuronas «blanco» se la llama transducción celular.
Se calcula que existen cien billones de células nerviosas. Cada célula se contacta a través de más de 5000 sinapsis, recibiendo cada neurona información aproximadamente de otras 1000 neuronas. De acuerdo a este cálculo, existirían 100 trillones de sinapsis cerebrales.
Los neurotransmisores están alojados dentro de vesículas para impedir que sus moléculas más elementales sean degradadas por las enzimas existentes en el botón terminal del axón. La vesícula sináptica con sus neurotransmisores químicos debe unirse a la membrana presináptica para poder liberar dichas sustancias en el espacio intersináptico. Se calcula que en un botón terminal axónico existen varios miles de vesículas, en cada una de las cuales se almacenan alrededor de cien mil moléculas de neurotransmisores. Del espacio intersináptico el neurotransmisor pasa a la membrana postsináptica, uniéndose a determinados sitios proteicos específicos llamados receptores.
El lugar donde un axón de una neurona se pone en contacto con otra célula o con dendritas de otras neuronas se denomina sinapsis. En este espacio intersináptico la transmisión del impulso se hace por medio de transmisores químicos, ya que ambas neuronas no se fusionan.
La neurona tiene un potencial de reposo de alrededor de -70 mV, la transmisión química (o eléctrica a veces) genera potencial sináptico inhibitorio (se hiperpolariza y se torna menos excitable) o uno inhibitorio (se depolariza y se hace más excitable).
Estas células y sus sinapsis son sumamente sensibles a la falta de glucosa y de oxígeno, así como a cualquier sustancia tóxica. Por esta razón el cerebro se halla separado de la circulación sanguínea general por la denominada «barrera hematoencefálica». Esta barrera consiste en un tejido compuesto por células (de la glia), fibras y una sustancia intercelular. Estas células neurales o astrocitos poseen expansiones terminales («pies perivasculares o chupadores») adheridos a la pared externa de los vasos sanguíneos cerebrales por un lado, y por el otro envuelven en forma de telaraña a las neuronas propiamente dichas.
1-5. Citoesqueleto, membrana plasmática
Los neurotransmisores deben ligarse al receptor para poder atravesar la membrana citoplasmática bilipídica, para ejercer su acción intracelular.
La mayoría de las actividades metabólicas celulares se realizan en la matriz citoplasmática o citosol. Esta matriz está compuesta de proteínas, tubulina y actina, cuyas función es darle forma y motilidad a la neurona.
Cada neurona tendrá un «microambiente fabricado» (citoesqueleto), especialmente para recibir un determinado neurotransmisor. Así existe, por ejemplo, un ARN mensajero nuclear, que se transfiere directamente a las dendritas postsinápticas, para efectuar la traducción (síntesis) de una proteína citoesquelética (AMP 2, microtubule associated protein) en la dendrita neuronal.
Aparte de esta matriz citoplasmática, existen en la neurona un sistema de endomembranas, que está compuesto por:
– el aparato de Golgi: órgano de procesamiento de productos del retículo endoplásmico,
– los endosomas: encargados de recibir o expulsar los materiales extra o endocelulares,
– los lisosomas: que contienen enzimas hidrolíticas,
– el retículo endoplásmico: donde están los ribosomas y
– la envoltura nuclear: que posee un pasaje porósico entre el núcleo y el citoplasma, donde existe una pared interna en contacto con los cromosomas y otra externa en contacto con los ribosomas),
La membrana plasmática está compuesta por fosfolípidos, colesterol y glucolípidos, de tal manera que las capas hidrofílicas se dirigen hacia la parte acuosa (medio extracelular) y las hidrofóbicas, se ponen perpendicularmente a la solución acuosa.
Los lípidos se disponen en forma de una doble capa, mientras que las proteínas lo hacen en una capa fluida hacia ambas superficies. La superficie de la membrana es asimétrica, sobresaliendo proteínas y oligosacáridos hacia afuera o hacia adentro de la célula. De esta forma la membrana actúa como barrera al pasaje de sustancias extraías y permite mantener la homeostasis intracelular.
Los glicerfosfolípidos son un tipo especial de fosfolípidos, formados a partir del fosfato y del glicerol. Los más conocidos son:
– fosfatidilcolina decitina),
– fosfatidiletanolarnida,
– fosfatidilserina, y
– fosfatidilinositol
Para que los psicofármacos ejerzan su acción deben atravesar esta capa bilipídica de forma activa (con consumo de energía), ya sea actuando sobre los neurotransmisores, o de manera directa sobre los receptores, para conseguir la migración informativa transmembránica y llegar al citosol (intraplasmático).
De estos grupos de fosfoglicéridos y de carbohidratos dependen las características hidrofílicas o hidrofóbicas de las diferentes caras o regiones de la biomembrana. Según el estado y las condiciones biológicas de estos componentes de membrana será posible o no el pasaje de las sustancias, pudiéndose conseguir o no los efectos psicofarmacológicos deseados.
Las alteraciones en la viscosidad y en la fluidez de membrana afectan directamente el proceso de acoplamiento del ligando endógeno: por más que la molécula del psicofármaco sea la adecuada no se obtendrá el efecto terapéutico, porque para que el psicofármaco ejerza su acción debe fijarse y acoplarse, de manera muy cuidadosa y prolija, sobre la superficie de la membrana.
Las dobles uniones de los ácidos grasos no saturados permiten que la membrana sea más flexible, en cambio el colesterol y las proteínas transmembranosas tienden a aumentar la rigidez, lo mismo que la disminución de la temperatura ambiente.
Cuando por malnutrición, envejecimiento o enfermedad orgánica, la membrana no se encuentre en buenas condiciones, no se obtendrá el efecto farmacológico deseado, porque no será suficiente la «adherencia», ni el proceso defosforilación.
El proceso defosfórilación es necesario para poder modular los efectos de los neurotransmisores que actúan sobre las sinapsis de la «neuronas targets o blanco» a corto plazo y es el mecanismo más importante de la neuroplasticidad neuronal. El otro mecanismo de transformación, a largo plazo, se logra mediante los cambios de le expresión genética.
La fosfórilación permite que la proteína cambie su tamaño y/o conformación por alteración de su carga debido a que los grupos fosfatos, que ceden el fósforo, están cargados de manera negativa. La proteína puede entonces, por ejemplo:
1) cambiar la permeabilidad de un canal iónico,
2) cambiar su afinidad por otras proteínas: la fosforilación de la tiroxinahidroxilasa incrementa la afinidad por su cofactor produciendo una aceleración en el ritmo de conversión de tirosina en dopa. La fosforilación de ciertas nucleoproteínas impiden la transcripción del ADN-ARN.
Los glucolípidos (gangliósidos y cerebrósidos) se constituyen a partir de la ceramida con galactosa o glucosa para los gangliósidos y con oligosacáridos en el caso de los cerebrósidos. La ceramida, constituyente fundamental de la esfingomielina, se forma a partir de un alcohol (esfingosina) con un ácido graso.
Precisamente, las investigaciones en la enfermedad de Alzheimer se desarrollan específicamente en relación a esta patología degenerativa de los glucolípidos (mielina, glucósidos monosacáridos, galactocerebrósidos, gangliósidos, etc.). Casi todos los nuevos desarrollos psicofarmacológicos en este campo se diseñan con el objetivo de proteger estos componentes de membrana (neuroprotectores, ver capítulo Psicofarmacología geriátrica).
El gangliósido GM2 por acción de la hexosaminidasa A, se transforma en gangliósido GM3. Esta enzima está en bajas concentraciones en la enfermedad de Tay-Sachs, que cursa con una acumulación de GM2 en el sistema nervioso central, con graves consecuencias neurocognitivas. Esta enfermedad junto con la de Gaucher (acumulación lipídica en hígado, bazo y médula ósea) y la de Nieman Pick se las conoce como enfermedades lisosomales, ya que la alteración el reside en la degradación de estos componentes de la endomembrana (62).
La regulación del glutamato y del ácido caínico [a través del receptor Al (NMDA, N-Metil-D-Aspartato) y del A3 (cainato)] con el calcio, son factores que se estudian para proteger los componentes de membrana. Un influx excesivo de estos compuestos perjudica sensiblemente a la membrana (ver más adelante 1-14.)
El colesterol, que también forma parte de la biomembrana, ha concentrado en los últimos años un enorme interés. Parece ser que de él depende, en forma destacada la fluidez de la membrana y la riqueza de los receptores. La distribución de colesterol en la célula no es homogénea y diferentes sistemas celulares funcionan merced a la participación del colesterol, como son por ejemplo la mielina, el plasma de membrana glial, el plasma de membrana, el axón, el núcleo, la sinapsis, los lisosomas, el retículo endoplásmico, el aparato de Golgi, entre otros.
El colesterol participa de procesos celulares directamente asociados a la respuesta psicofarmacológica. Dietas bajas o muy bajas en colesterol podrían afectar la respuesta a los psicofármacos. Asimismo el descenso brusco de la tasa de colesterol podría afectar al comportamiento humano, elevando las tasas de suicidio e incrementando los niveles de violencia o muertes por accidentes (10).
Si bien el oxígeno y las sustancias químicas de molécula muy pequeña pueden difundirse libremente a través de la membrana celular de los vasos sanguíneos, de las células de la glia y de las neuronas, sustancias algo más complejas, como la glucosa o los psicofármacos, necesitan de un transporte activo enzimático o ser altamente liposolubles para poder atravesar las membranas y llegar a la neurona donde ejercen su acción. Normalmente, la célula nerviosa posee un potencial eléctrico negativo de 70 milivoltios respecto del exterior.
Ello es debido a que permite la entrada de iones de potasio y elimina activamente los iones de sodio (bomba de sodio).
Esta «bomba» la constituyen proteínas que cambian su estructura para permitir la entrada o salida de los iones. Este trabajo se realiza con un gasto de energía que queda almacenada en el ácido adenosintrifosfórico (ATP). Cuando la célula «dispara» el impulso -como respuesta a la información recibida del exterior a través de sus dendritas- permite que el sodio entre en el axón, cambiando su potencial eléctrico de negativo a positivo (potencial de acción), propagándose así el impulso.
Cuando el impulso llega a la parte dilatada final del axón (botón terminal axónico) libera sustancias químicas que están almacenadas dentro de vesículas protectoras, y logra cumplir así el objetivo de transmitir la información a la célula nerviosa vecina. Dado que la amplitud del impulso es la misma, a mayor cantidad de impulsos habrá mayor liberación de moléculas de las sustancias, llamadas neurotransmisores.
La afinidad se puede medir por la concentración del ligando que ocupa la mitad del total de receptores disponibles (constante de disociación, Kd). Los Ki moles (nmoles) es la concentración a la que la droga produce el 50 % de inhibición (ver más adelante en caps, 3 y 6 la potencia clínica del psicofármaco, en relación a los efectos terapéuticos/ adversos, producto de este bloqueo).
Los psicofármacos con mayor afinidad se unirán al receptor con menores concentraciones y viceversa, constituyendo ello la base del reconocimiento molecular.
1-6. Receptores
El neurotransmisor (primer mensajero) se liga al receptor proteico y atraviesa la membrana citoplasmática a través de los canales iónicos o por intermedio de las proteínas G transmembranosas.
Los receptores son proteínas hidrofóbicas en contacto con los capa bilipídica de la membrana celular, que reconocen, fijan al neurotransmisor y tienen la función de informar a otros sistemas, a través del pasaje de la información. Se encuentran a ambos lados de la sinapsis (pre y postsinápticos).
En sus extremidades se encuentran campos hidrofílicos. La cara interna del receptor está en contacto con el complejo de primera membrana, donde se desarrollan procesos de fosforilación que transducirán información desde la cara externa del receptor hacia la región citosólica (parte del citoplasma donde se encuentran las endomembranas). La cara externa del receptor presenta áreas de glicocilación. Esta cara externa se unirá a ligandos endógenos o exógenos.
Los subtipos de receptores están determinados por las subunidades de las proteínas que los forman. Estas proteínas pueden ser monoméricas o poliméricas.
El concepto de bimodalidad del receptor está determinado porque el mismo tiene funciones de recepción del ligando exógeno o endógeno: sensibilidad, afinidad, velocidad, concentración y distribución (Bmax, Kd, Vmax). De esta forma las drogas de diseño, se sintetizan de acuerdo a la estructura molecular del receptor.
Se han descubierto dos subtipos de proteínas en la parte terminal del axón, sinapsina lA y IB asociadas a las vesículas sinápticas. Ambas son el sustrato para los segundos mensajeros de proteinoquinasas AMP cíclico dependientes y para el complejo calcio-calmodulina, interviniendo, por su rapidez de fosforilación, en la liberación de la vesícula sináptica.
1-7. Receptores hetero-oligómeros o ionotrópicos
Las bombas de los receptores iónicos (Ca, lí, Na, ATPasa) permiten mantener un potencial negativo intracelular, con respecto al medio extracelular.
Son receptores que a través del canal iónico desplazan en forma autónoma y veloz la información, sin depender de la proteína G. Algunos receptores pueden estar heteroligados funcionalmente, es decir, pueden depender del canal iónico por un lado y de la proteína G por el otro.
Los receptores ionotrópicos están formados por diferentes uniones proteicas, con una homología que varía entre el 70 y 80 %. El conjunto de subunidades funciona con un concepto de bimodalidad. Por un lado las subunidades representan sitios de acción y de fijación para los ligandos, y por otro lado, el conjunto coronal de subunidades formalizan anatómicamente la estructura anatomofuncional del canal iónico.
Al ser polimérico, los ligandos que ejerzan acción sobre este receptor, no necesitarán lo que se conoce como tiempo de latencia, como lo necesita el receptor monomérico dependiente de la proteína G. Un ejemplo de este tipo de receptores, es el receptor benzodiacepínico.
La membrana es impermeable a los iones, siendo necesario el consumo de energía para mantener el gradiente negativo intracelular. La entrada de iones cargados positivamente (cationes) hacen que la membrana disminuya su potencial negativo (receptor nicotínico de acetilcolina), es decir que al despolarizarse, permite aumentar la excitabilidad neuronal (neurotransmisores excitatorios).
Por el contrario los iones cargados negativamente (aniones) producen una hiperpolarización, el interior celular es más negativo (receptores gaba-cloro) y disminuye su excitabilidad (neurotransmisores inhibitorios).
1-8. Receptores monoméricos o metabolotrópicos
El receptor, activado por el neurotransmisor (primer mensajero), modifica la conformación de la proteína G y produce la formación de numerosas moléculas de AMP cíclico, diacilglicerol, e inositoltrifosfato (segundos mensajeros), cuya consecuencia es una intensa amplificación de la señal originada en el receptor.
También conocidos como receptores de acción indirecta o acoplados a la proteína G (GTP-binding protein). Estos receptores están localizados del lado citosólico de la membrana celular.
Para difundir a través de las membranas bilipídicas, las moléculas hidrofílicas, deberán unirse a un receptor tipo relacionado con la tipo proteína G. Esta proteína está compuesta de tres subunidades: la alfa que está ligada al GDP o GTP, a través de la GTPasa y la beta y gama que queda unida a la membrana.
Existen proteínas G estimuladoras (Gs y Gq) e inhibidoras (Gi). El ligando exógeno al tomar contacto con la subunidad alfa debilita su unión con el GDP y es reemplazado por la GTP.
La activación de la proteína G divide la subunidad beta-gama de la alfa que se desplaza por la membrana plasmática y puede activar a los 2dos. mensajeros AAW o G7Psegún active la adenito ciclasa o lafosfotipasa G respectivamente.
El segundo mensajero, nucleótido AMP cíclico se genera a partir del ATP, al combinarse con la ribosa y tiene por objetivo activar a la proteionoquinasa. A que provoca una estimulación celular por fosforilaciones sucesivas. Es inhibido por la proteína Gi.
El GTP es hidrolizada a GDP y fosfato por la GTP asa que al terminar de estimular permite que la subunidad alfa vuelva a unirse con la beta-gama nuevamente.
La fosfolipasa C genera los segundos mensajeros diacilglicerol (DAG) y e inositol 1, 4,5 trifosfato (IP3) a partir delfosfatidilinositol 4,5 difosfato (PIP2).
La liberación de IP3 en el citoplasma de membrana provoca la liberación de calcio del retículo endoplasmático, que al actuar conjuntamente con la calmodulina, es capaz de combinarse con diferentes proteínas, en tanto que el DAG activa las proteinoquinasas (M).
Los segundos mensajeros producen la estimulación directa o indirecta de las PK, fosforilando las proteínas e induciendo cambios en el proceso excitatorio neuronal (22).
La proteína G amplifica señales debido a que una sola molécula de proteína G es capaz de activar a numerosas moléculas de adenilatociclasa y producir gran cantidad de AMP cíclico.
De esta forma la proteína G produce a través del AMP cíclico, diferentes efectos celulares en numerosos órganos: el estímulo de la LH sobre el ovario aumenta la producción de estrógeno y progesterona; el estímulo de la adrenalina sobre el receptor alfa 2-adrenérgico activa la proteína Gi, inhibe la adenilatociclasa, hiperpolariza la membrana (cierra los canales de K), produce menos AMP cíclico y termina con el efecto relajante del músculo liso intestinal y bronquial.
1-9. Receptores citoplasmáticos
Los esteroides tienen receptores citoplasmáticos y pasan directamente al núcleo para su transcripción en el ARN.
Existen moléculas hidrofóbicas (hormonas esteroideas -estrógenos, andrógenos, cortisol-, tiroideas) que pueden activar los receptores citosólicos de manera directa. Una vez ligado al receptor pasa al núcleo donde al unirse a un gen específico forma un ARN mensajero, que luego se traducirá en la síntesis de una determinada proteína.
1-10. Receptores ensimáticos
El óxido nítrico es un neurotransmisor gaseoso de alta velocidad, se une a la enzima guanilato ciclasa en el citoplasma y produce GMP cíclico.
El óxido nítrico es un neurotransmisor gaseoso de tipo paracrino (de corta distancia), producido por las neuronas, los macrófagos y el endoterlio capilar. Se genera a partir de la arginina, del oxígeno y de la NADPH, a través de la óxido-nítrico-sintetasa (NOS). Difunde libremente en el citoplasma celular y actúa sobre la guanilato ciclasa que produce GMP cíclico que se convierte en el segundo mensajero. También actúa sobre la dilatación de los vasos sanguíneos peneanos durante la erección al producir la relajación del músculo liso velozmente.
1-11. Signal path-way
Existen caminos moleculares, del citosol al núcleo, que pueden ocasionar un cambio en la transcripción genética.
Bajo este nombre se conoce el camino de la neuromodulación que rige desde el acople del ligando exógeno o endógeno al sitio de recepción y desde éste a la red informativa de carácter centrípeto que viaja desde el citosol al núcleo. En el caso del litio, el signal patway es citosólica prenuclear: inhibe la relación IP3-diacilglicerol; en el de la heroína es intranuclear, ya que va produciendo modificaciones intracitosólicas, cuya repetición producirá a través de mecanismos de recodificación genética, alteraciones del ADN que influirán en el anteproyecto o blue print celular.
1-12. Resumen
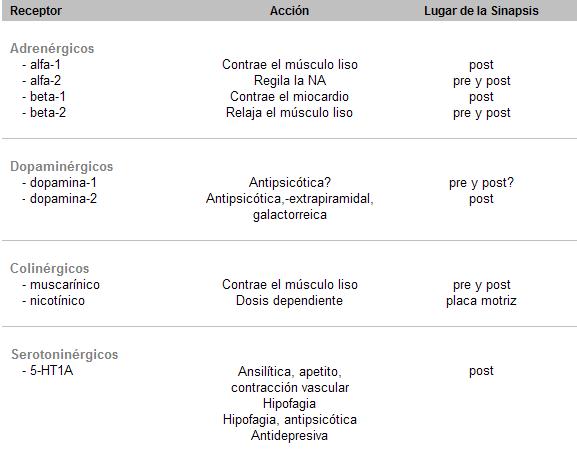
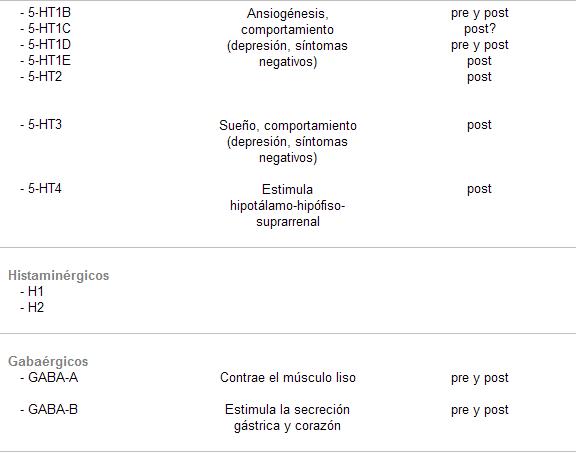
Los receptores presinápticos se denominan autorreceptores y regulan la liberación del neurotransmisor. En la postsinapsis existen varios tipos de receptores para un mismo transmisor; por consiguiente, la respuesta dependerá sobre cuál tipo de receptor actúa un mismo neurotransmisor.
La transducción es el proceso de unión del neurotransmisor (primer mensajero) con el receptor Tiene como objetivo la transmisión de la información al AMPc, GMPc, Ca, DAG, IP3 (segundos mensajeros) -que luego deben fosforilar a proteinoquinasas más complejas (terceros mensajeros)-, para poder continuar con el mensaje, hasta almacenarlo en el núcleo (factores de transcripción ARNm, cuartos mensajeros) y producir alguna señal, como respuesta celular
Esta transducción se puede realizar:
a. Por canales iónicos, que permitan la entrada y salida de diferentes iones (sodio, potasio, calcio, etc.).
b. Por sistemas enzimáticos, que al activarse o inhibir a otras enzimas (unidades catalíticas), forman los segundos mensajeros que actúan a través de:
– la conversión de ATP en AMP cíclico
– la conversión de GTP en GMP cíclico
Esta unidad catalítica estaría entonces formada por el receptor, la unidad catalítica ATP – AMPc y una unidad reguladora de guanosina trifosfatoguanosina monofosfato (GTP-GMP).
La proteína G podría ser estimuladora o inhibidora según a qué tipo de receptores se acople.
El GMP cíclico es sintetizado por la enzima guanilatociclasa. El calcio (segundo mensajero) está directamente asociado a la transmisión intracelular rápida y de corta duración; su aumento intracitoplasmático puede ser tóxico.
Todo ello es necesario para lograr atravesar la membrana citoplasmática y llegar al núcleo celular Camino que es posible luego de pasar por el citosol o matriz citoplasmática y/o por el sistema de endomembranas.
1-13. Mecanismos de acción de los psicofármacos según su sitio de acción en la sinapsis
Los psicofármacos actúan a nivel de las vesículas presinápticas, inhiben o estimulan los receptores pre o post-sinápticos y/o bloquean y/o estimulan la recaptación de neurotransmisores.
El sitio de acción de los psicofármacos es la sinapsis. Cada uno de los diferentes neurotransmisores puede ser alterado por los psicofármacos, consiguiéndose así inhibir o excitar las neuronas de acuerdo con el fármaco utilizado. Se puede esquematizar la acción de los psicofármacos como una interferencia que abarca desde la formación hasta la degradación de los neurotransmisores:
1) Inhibición de la síntesis. Si se inhibe la enzima dopa-decarboxilasa, la dopa no se transformará en dopamina, impidiéndose así la síntesis de noradrenalina. De esta forma, actúa el antihipertensivo alfa-metildopa que provoca una inhibición de la síntesis catecolamínica y una reducción de los efectos presores periféricos. Se obtiene además un efecto sedante.
2) Producción de neurotransmisores falsos e inefectivos. Siguiendo el ejemplo anterior, la alfa-metildopa se convierte, por acción de la dopa-decarboxilasa, en alfa-metildopamina y alfa-metilnoradrenalina. Estas dos sustancias, al reemplazar de forma equimolecular a la dopamina y a la noradrenalina, y ocupar los lugares de los receptores postsinápticos correspondientes a estos dos neurotransmisores, impiden su acción.
3) Depleción de los neurotransmisores intracelulares. Se pueden deplecionar los depósitos de noradrenalina existentes en las vesículas del botón axónico terminal, e impedir de esta manera la liberación de catecolaminas. Un ejemplo de esta acción lo constituye la reserpina. Hasta hace algunos años era usada para conseguir efectos antimaníacos y sedativos en los procesos esquizofrénicos. Esta acción deplecionante era útil por su efecto antihipertensivo (efecto reserpínico).
4) Inhibición de la liberación del neurotransmisor. El agente antihipertensivo guanetidina interfiere en la liberación de la noradrenalina en el espacio intersináptico.
5) Incremento de la liberación del neurotransmisor La anfetamina y sus derivados incrementan la liberación de catecolaminas y otros agentes simpaticomiméticos en el espacio intersináptico. De esta forma provocan acciones excitantes centrales.
6) Inhibición de la monoaminooxidasa intracelular. En la actualidad se han descubierto dos diferentes monoaminooxidasas (MAO). La MAO «A», que deamina la serotonina, la dopamina, la tiramina y la octopamina, y la MAO «B», que deamina la feniletilamina, la tiramina y la dopamina. La MO «B» se encuentra predominantemente en el sistema nervioso central.
Los inhibidores de la MAO «A» y la MAO «B» provocan una mayor disponibilidad de sustancias cate colamínicas, para ser liberadas en el espacio intersináptico.
7) Inhibición de la recaptación. La recaptación de catecolaminas y de otras sustancias químicas en el botón sináptico representa una vía económica para la neurona, que almacena nuevamente el neurotransmisor no utilizado.
Un gran número de psicofármacos, principalmente los antidepresivos tricíclicos, bloquean este mecanismo. Se consigue así una mayor disponibilidad de neurotransmisor a nivel de la sinapsis, lográndose la producción de un efecto excitatorio catecolamínico (efecto cocaínico).
8) Estimulación del receptor. No es una acción habitual. La apomorfina estimula los receptores dopaminérgicos, provocando una acción vomitiva específica, que encuentra aplicación terapéutica en las intoxicaciones agudas.
9) Bloqueo del receptor. Es el mecanismo habitual de los neurolépticos. Bloquean los receptores dopamínicos postsinápticos, provocando una disminución de los impulsos excitatorios a nivel del sistema nervioso central.
1-14. Neurotransmisores
Los neurotransmisores (ligandos) actúan sólo en las sinapsis: las células inductoras que los secretan se hallan en contacto directo con las células inducidas o blanco que los reciben. Se clasifican de acuerdo a su origen y tipo de acción.
En los últimos años se ha podido demostrar que los transmisores sinápticos pueden diferenciarse no solamente por sus acciones, sino también por las características de las respuestas que provocan (rápidas o lentas), por las distintas estructuras químicas (simples o complejas), por el peso molecular (alto o bajo), por la preponderancia de las respuestas químicas o eléctricas, etc.
Las respuestas químicas que actúan sobre receptores químicos específicos (tienen especificidad) e inducen un determinado tipo de acción (tienen eficacia). La célula que secreta el ligando (célula inductora) está en contacto con la que recibe el ligando (célula inducida o blanco). Cuando la secreción del ligando se encuentra cerca de las células blanco se denomina secreción paracrina, si es secretado y recibido por la misma célula se llama secreción autocrina.
De acuerdo con estas diferentes particularidades se los ha denominado neurotransmisores (respuestas rápidas, la célula inducida está en íntimo contacto con la célula blanco), neuromoduladores (respuestas lentas), neuromediadores (respuestas de tipo postsináptico), neuropéptidos (transmisores de alto peso molecular), neurohormonas (moduladores de la secreción de otras hormonas: la célula inducida está distante de la célula blanco). Sin embargo, muchas veces las acciones se superponen, por lo que los límites de cada una de estas categorías resultan imprecisos.
Los neurotransmisores se caracterizan por estar presentes en el sistema nervioso central y por tener mecanismos propios de síntesis, almacenamiento, degradación, recaptación e inactivación. Además, deben poseer receptores específicos a los cuales puedan bloquear los fármacos. Este tipo de neurotransmisores provoca respuestas químicas y eléctricas.
Las respuestas eléctricas pueden ser excitatorias o inhibitorias. Las excitatorias producen un potencial postsináptico excitatorio, que origina una despolarización neuronal con ingreso de sodio y egreso de potasio intracelular hasta que se logra un nuevo equilibrio, merced a la bomba de la Na-K-ATPasa, que finalmente limita la propagación del impulso.
Si la respuesta es de tipo inhibitorio, se produce un potencial postsináptico inhibitorio que provoca la entrada de cloruro a la neurona y ocasiona la hiperpolarización, hasta lograr un nuevo equilibrio.
La respuesta dependerá de la sumatoria de ambos procesos (excitatorios e inhibitorios), que la neurona recibe simultánea y constantemente. Muy pocos neurotransmisores satisfacen todos estos criterios. Se los clasifica en:
– Neurotransmisores verdaderos.
– Neurotransmisores putativos. Son los que no satisfacen todos los criterios que
permitirían considerarlos neurotransmisores verdaderos.
– Autorreceptores o receptores presinápticos. Se caracterizan por ser sensibles a las concentraciones del neurotransmisor en la biofase de la sinapsis, regulando así, por un mecanismo de feedback o retroalimentación, la liberación o el bloqueo del neurotransmisor en juego.
Los neuromediadores son transmisores químicos que aumentan las respuestas postsinápticas sin originar respuestas eléctricas. Se los ha denominado segundos mensajeros (adenosina, adenosinmonofosfato cíclico, guanosinamonofósfato cíclico).
Los neuromoduladores son sustancias complejas cuya acción desencadena cambios lentos a mediano y largo plazo. Ejercen influencia sobre los neurotransmisores. Se originan en sitios neuronales o extraneuronales (prostaglandinas, factor de crecimiento neuronal).
Los inmunoneuropéptidos son polipéptidos que se originan en las neuronas del hipotálamo y áreas vecinas. Los polipéptidos se caracterizan por ser condensaciones de varios aminoácidos, cuyas uniones se realizan entre los grupos amino y ácido de sus extremos. Los dipéptidos o tripéptidos se asemejan en sus propiedades a los aminoácidos, en tanto que los polipéptidos presentan mayor semejanza con las proteínas. Arbitrariamente se llama polipéptidos a los que presentan un peso molecular inferior a 6000, y proteínas, a los de peso molecular mayor.
A estos péptidos se los llama neurohormonas cuando producen liberación de hormonas «tróficas o trópicas», es decir, de hormonas que actúan sobre las glándulas periféricas donde se elaboran hormonas específicas, las que a su vez, por un mecanismo de feedback, estimulan o frenan la producción de las trofinas
correspondientes.
Estas hormonas «trópicas» hipofisarias están bajo la influencia de un factor neurohormonal liberador (releasing) y por otro inhibidor (inhibiting), cuyas acciones sumadas algebraicamente, con el agregado de componentes psicológicos (mediados por neurotransmisores, neuromediadores, etc.) y por componentes hormonales propiamente dichos (mediados por la hormona periférica específica con su feedback positivo o negativo), originan una determinada respuesta (ver cap. 2).
Los neurotransmisores más importantes son:
Catecolaminas
Se denomina así a la adrenalina, la noradrenalina y la dopamina, porque las tres derivan del núcleo catecol, cuyo origen son los aminoácidos fenilalanina y tirosina.
Estas aminas son de fundamental importancia en las reacciones de alarma, adaptación e inhibición. La alteración de su síntesis o de su degradación ha sido vinculada a los desórdenes afectivos y la enfermedad esquizofrénica. Se puede registrar actividad catecolamínica con aumento del flujo sanguíneo en los músculos antes que éstos muestren actividad eléctrica. La vasoconstricción que las catecolaminas provocan sirve para enviar flujos sanguíneos a áreas más necesitadas. Están distribuidas de forma amplia dentro y fuera del sistema nervioso central. En el sistema nervioso central la noradrenalina se concentra en el hipotálamo y las estructuras subtalámicas.
La dopamina se halla de forma preponderante en los núcleos de la base.
A nivel periférico, la noradrenalina se localiza principalmente en las fibras simpáticas posganglionares. La adrenalina se halla en la médula adrenal, en las células cromófilas que forman el conjunto celular APUD (amine precursor uptake and decarboxilation). La dopamina a nivel periférico se encuentra en el aparato sanguíneo renal.
La conversión de L-dopa en dopamina por la enzima dopa-decarboxilasa es necesaria para poder atravesar la barrera hematoencefálica y ejercer así su acción en el sistema nervioso central. La dopamina, a nivel de los ganglios de la base, posee una acción contraria a la de la acetilcolina. La falta de dopamina provoca efectos nerviosos centrales caracterizados por movimientos musculares involuntarios, depresión, confusión, alucinaciones, etcétera.
Alrededor del 40 % de las catecolaminas se encuentra en forma libre dentro del citoplasma celular. El 60 % restante se halla almacenado en forma de gránulos en las vesículas situadas en los botones axónicos terminales. De esta forma no son degradadas por la monoaminooxidasa (MAO) intracelular.
El efecto alfa de las catecolaminas fue definido como vasoconstrictor y estimulante de la contracción del músculo liso, con excepción del músculo gastrointestinal (receptor vascular alfa-1 postsináptico).
El efecto beta se caracteriza por la relajación que provoca en el músculo liso y por el aumento de la contractilidad miocárdica.
Actualmente se diferencian además un receptor beta-I, que sería el responsable de las acciones cardíacas y lipolíticas, y un receptor beta-2, que favorecería la broncodilatación y la vasodilatación.
La clonidina y la guanafacina son agonistas alfa-2 (presinápticos); la yohimbina y el piperoxán son antagonistas.
Los agonistas de los receptores beta-1 son la noradrenalina, el prenanterol y la dobutamina; en cambio el metroprolol y el propranolol son antagonistas.
La adrenalina, el salbutamol y el clembutorol son agonistas de los receptores beta-2, cuyo antagonista es la butoxamina.
Los receptores beta han sido localizados también en la neuroglia. Se desarrollan de forma independiente los receptores beta-I, que son presinápticos y activados por la noradrenalina, de los beta-2, que son activados por la adrenalina.
La clonidina es estimulante de los receptores alfa-2 presinápticos y disminuye la liberación de noradrenalina por una regulación descendente.
Los receptores beta-adrenérgicos estimulan la adenilciclasa a través de la proteína Gs, produciendo un aumento en la concentración del AMPc y la fosforilación de diversas proteínas.
En cambio, los receptores alfa-adrenérgicos inhiben la adenilciclasa e interactúan con la proteína Gi, por lo que reducen las concentraciones de AMPc.
La estimulación de los receptores alfa aumenta las concentraciones de calcio por activación de la fosfolipasa C, por medio de la proteína G, y se generan dos segundos mensajeros: el inositol trifosfato (IP3) y el diacilglicerol (DAG).
La estimulación de las vías dopaminérgicas corticales estaría relacionada con la aptitud, la agitación y el aprendizaje. El bloqueo de estas vías produciría inmotivación, decremento de la tensión y adinamia.
La hiperquinesia se desarrolla por estimulación del área nigroestriada, y su bloqueo produce disquinesia tardía, hipoquinesia y rigidez.
Los receptores presinápticos están relacionados con la modulación de la regulación de dopamina a través de un feedback negativo, y estarían localizados en la región prefrontal y, con menor densidad, en las regiones corticales y mesolímbicas.
El receptor de dopamina 1 (DAI) está asociado y ligado al sistema adenilciclasa, se une a la apomorfina y es regulado por la guanosina trifosfato (GTP).
Al receptor dopamina 2 (DA2) se lo encuentra en la región corticoestriada, no depende de la adenilciclasa, se liga a las butirofenonas y bloquea la liberación de la prolactina (ver cap. 2).
Los neurolépticos bloquean ambos receptores, algunos de forma más específica que otros. Así, por ejemplo, en concentraciones bajas la sulpirida o la pimozida actuarían más sobre los receptores postsinápticos que sobre los presinápticos.
En bajas concentraciones, la apomorfina y la bromocriptina estimulan los receptores presinápticos, y producen un decremento dopaminérgico, aunque sean agonistas dopaminérgicos.
En la esquizofrenia de tipo 1 se ha encontrado una hipersensibilidad del receptor DA2, y en la de tipo II, una hiposensibilidad de los DA1 y DA2.
Las hiperdopaminergias estarían ligadas a esquizofrenias productivas y de mejor pronóstico, mientras que las hipodopaminergias, a esquizofrenias con embotamiento afectivo y retardo psicomotor de peor pronóstico.
Se pueden obtener resultados de acciones antipsicóticas sólo cuando se bloquea el 80-90 % de los receptores DA2, al igual que en la enfermedad de Parkinson, en la que se necesitan amplias destrucciones de la vía nigroestriada para que aparezca sintomatología clínica.
Los receptores DA2, DA3 y DA4 son presinápticos postsinápticos, y están unidos de forma negativa a la proteína Gi y a la inhibición de la actividad de la adenilciclasa, en tanto que los receptores DA1 y DA2 tienen alta y baja afinidad, respectivamente.
La acción antipsicótica estaría más ligada a los receptores de DA2, de allí la investigación de nuevas drogas con mayor potencia anti-DA2 específica (amilsuprida, remoxiprida, pimozida). La ventaja de estos compuestos sería su relativa especificidad para bloquear receptores DA2 del sistema límbico, en lugar de los del cuerpo estriado.
Los autorreceptores de las neuronas dopaminérgicas que se encuentran en la parte somatodendrítica regularían los potenciales de acción y la síntesis proteica, en tanto que los de la parte preterminal del axón controlarían el flujo de la dopamina en la sinapsis.
La apomorfina, en dosis bajas, estimula al autorreceptor (inhibe la síntesis de dopamina y provoca la disminución de la actividad motora de las ratas) y en dosis altas estimula al receptor de dopamina postsináptico.
Se encuentran en la corteza prefrontal y el cíngulo. Las regiones mesolímbica y mesocortical carecen de este tipo de neuronas reguladoras.
Los agonistas del autorreceptor DA, con alta afinidad por los receptores postsinápticos, producen pocos efectos extrapiramidales; provocan una disminución de la actividad dopaminérgica en regiones mesolímbicas.
La estimulación de los receptores somatodendríticos también podría producir un decremento en la liberación de dopamina. Esto es una respuesta interesante para la investigación, ya que se presume una hiperfunción dopaminérgica mesolímbica o mesocortical en la esquizofrenia, que podría antagonizarse con agonistas DA2 y DA3 (talipexole y roxindole).
La noradrenalina tiene efectos predominantes alfa, la adrenalina efectos alfa y beta, y en la dopamina predominan los efectos beta.
Como todos los neurotransmisores, las catecolaminas liberadas en el espacio intersináptico pueden tomar diferentes caminos, una vez que algunas moléculas se han unido al receptor:
a) Pueden ser recaptadas (reuptake), para ser nuevamente almacenadas dentro de las vesículas en forma granular (mecanismo más importante).
b) Pueden ser metiladas por la enzima cometiltransferasa (COMT), presente
en el citoplasma celular, y de esta forma ser inactivadas.
c) Pueden pasar a la circulación general para ser deaminadas por la monoaminooxidasa (MAO) hepática y, de esta manera, excretadas en forma de metabolitos inactivos.
d) Pueden ser recaptadas y destruidas por la MAO mitocondrial.
Los metabolitos inactivos de la noradrenalina son el ácido vainillilmandélico, la normetanefrina y la metanefrina, que representarían a la noradrenalina de origen periférico. El 3-metoxi-4-hidroxifenilglicol (MOPEG) es el metabolito principal de la noradrenalina de origen central.
El ácido homovalínico constituye el metabolito inactivo de la dopamina. Todos estos metabolitos pueden ser dosados cuantitativamente en la orina y en el LCR, y sirven como parámetros en el estudio del metabolismo catecolamínico. La fosfodiesterasa, que degrada al AMP cíclico, puede ser bloqueada por sustancias como la teofilina o los mal llamados vasodilatadores cerebrales como la cinarizina o la pentoxifilina. Por consiguiente, estas drogas pueden considerarse potenciadoras de la acción de las catecolaminas.
En un estudio que realizamos en 18 pacientes con esquizofrenia, para determinar marcadores biológicos en la esquizofrenia I y II se pudo comprobar que, cuando se analizó el ácido fenilacético total (AFAT) se lo encontró disminuido en 8 pacientes, 5 pertenecían al tipo II, 2 al tipo III y 1 al tipo I. Es significativo que siendo el AFAT un marcador de rasgo de los trastornos depresivos, aparezca con valores bajos en esquizofrénicos de tipo II, que presentan un hipodopaminergia marcada, aunque comparten algunos síntomas de los trastornos afectivos (aplanamiento afectivo, retracción social, embotamiento y enlentecimiento psicomotor) (9).
Desde el punto de vista bioquímico, el AFAT pertenece al grupo derivado de la fenilalanina, del cual se desprenden los derivados de sustitución como son la noradrenalina, dopamina, tiramina y metabolitos intermedios de la formación de catecolaminas. Por acción de la decarboxilasa sobre la fenilalanina, se forma la feniletilamina y por acción de la XIAO sobre esta última, el ácido fenilacético.
Los pacientes que presentaron valores bajos de AFAT y sintomatología tipo II, serían candidatos al abordaje psicofarmacológico combinado de neurolépticos con antidepresivos, si bien se señala que esta combinación, debe ser realizada con cuidado, ya que los antidepresivos pueden exacerbar los síntomas psicóticos latentes.
La disfunción de las áreas cortico-subcorticales y la sintomatología de tipo I, se originarían en la alteración de la trasmisión dopaminérgica subcortical, debido a un input dopaminérgico aberrante de las neuronas de las estructuras mediales y temporales, que se consideran ligadas a diferentes factores genéticos (virales, noxas teratogénicas, etc.).
Un exceso del input dopaminérgico proveniente de las áreas límbico-temporales, podría producir una destrucción de la transmisión dopaminérgica subcortical. Es evidente entonces, que en la esquizofrenia de tipo 1 existan alteraciones por un hiperdopaminergia, que podría a su vez corresponderse o no con un exceso de ácido fenilacético.
Entre los resultados que hemos encontrado en los 26 pacientes con esquizofrenia, respecto a la medición de la MAO, se destaca la aparición de valores globales bajos tanto de la NIAO plaquetaria, como de la plasmática).
Una disminución de la MAO permite una menor degradación de dopamina y serotonina, que se correspondería con una excesiva estimulación de las estructuras ganglionares.
Dado que la nicotina aumenta la liberación de dopamina, desde el estriado y el núcleo accumbens, es conveniente restringir el uso del tabaco en pacientes esquizofrénicos que presentan valores disminuidos de MO, ya que altos niveles de nicotina y bajos niveles de la actividad de la MO, podrán potenciar la sintomatología del tipo 1.
Los antidepresivos de tipo IMAO estarían contraindicados en esquizofrénicos que presenten valores bajos de MO, ya que los mismos podrían potenciar, por incrementar la vía dopaminérgica, la aparición de síntomas psicóticos.
Diversos estudios por radioimágenes (PET, SPECT), demostraron una Pobre activación de la perfusión dorso lateral del cortex prefrontal en los pacientes esquizofrénicos, que se correlaciona con niveles bajos de ácido homovaníllico (FIVA) y ácido 5-hidroxiindolacético en LCR: a menores niveles de ácido homovanílico, mayor severidad de síntomas negativos; una hiperfunción dopaminérgica estaría asociada con síntomas positivos y una hipofunción dopaminérgica con síntomas negativos. En pacientes con sintomatología positiva existe un hiperflujo metabólico en el área subcortical y un hipoflujo en el área frontal, en tanto que en los que presentan síntomas negativos existe un hipermetabolismo cerebral global con un descenso marcado del ácido homovaníllico en LCR.
Serotonina o 5-hidroxitriptamina
La importancia de este neurotransmisor comenzó a ser reconocida cuando se investigó la fisiología del sueño. Sería un modulador del sueño, de la actividad sexual y de la conducta agresiva. El ácido lisérgico (LSD) es un antagonista de la serotonina; provoca alucinaciones, así como un proceso de desincronización del electroencefalograma realizado durante el sueño en adictos al LSD.
La serotonina, a diferencia de las catecolaminas, tiene su origen en un núcleo indólico, y su precursor es el triptófano; su principal metabolito inactivo es el ácido 5-hidroxiindolacético. Aumenta la liberación de ACTH, hormona de crecimiento y prolactina e inhibe la FSH, LH y TRH. Puede inhibir o liberar la MSH y es un precursor de la hormona de la glándula pineal (melatonina).
El triptófano participa activamente en la formación de ácido nicotínico, compuestos indólicos y serotonina. Es convertido, por hidroxilación, a 5hidroxitriptófano y luego, a través de la decarboxilasa, se convierte en 5hidroxitriptamina (5-HT, serotonina). La MO la degrada a 5-hidroxiindolacético (5-HIA).
Su principal localización es en el núcleo del rafe. Existen numerosos subtipos de 5-HT en estudio, de los cuales los más conocidos son 5-HT1 (A, B, C y D), 5-HT2 y 5-HT3.
La disminución de la serotonina en el LCR ha sido ampliamente relacionada con los trastornos obsesivo-compulsivos y las conductas suicidas,
La concentración baja de 5-HIAA en el LCR de pacientes que realizaron intentos suicidas es un marcador de próximos intentos.
Además, la 5-HT poseería un efecto inhibidor gonadotrófico, con la consecuente pérdida de la libido o estímulo sexual, efecto que está apareciendo de forma más notable con el uso masivo de los antidepresivos inhibidores de la recaptación de serotonina (IRSS).
El efecto negativo de la serotonina consistiría en bloquear la conversión del triptófano en vitamina B3 (ácido nicotínico), con la consiguiente disminución de las coenzimas I y II (nicotinamida-dinucleófico [NAD] y nicotinamidafosfato-dinucleótico [NADP]). Ello provocaría también trastornos en el metabolismo hidrocarbonado y graso, con deterioro de la actividad mitocondrial y disminución de la producción de MAO. Algunos autores señalan que esta vía de transmetilación se encuentra en individuos normales; por ello se pueden detectar en la orina concentraciones muy bajas de estas sustancias. En episodios esquizofrénicos agudos, el aumento de la cantidad de estos compuestos es considerable, pero decrece rápidamente. La ingesta de triptófano y metionina podría estar relacionada con la producción de estas sustancias psicotomiméticas, pero los estudios realizados con dietas carentes de estos aminoácidos en pacientes esquizofrénicos no han dado resultados terapéuticos valederos.
Otro hecho que corrobora esta hipótesis es la escasa diferencia entre las psicosis tóxicas por estimulantes del tipo anfetamínico (anfetaminas, metilfenidato, cocaína) y el episodio paranoide agudo de una esquizofrenia. Si bien algunos autores tratan de diferenciarlos clínicamente por la presencia de alucinaciones visuales, táctiles y olfatorias (más comunes en la psicosis anfetamínica que en la psicosis esquizofrénica), desde el punto de vista clínico ambas son similares.
En individuos «normales», bajas dosis de estos estimulantes sólo provocan hiperactividad, en tanto que altas dosis remedan la esquizofrenia paranoide.
Las anfetaminas o sus derivados pueden ser transmetilados por la enzima N-metiltransferasa. Además, las anfetaminas provocan la liberación de catecolaminas e inhiben la MAO, existiendo así una mayor probabilidad de formación de compuestos psicotomiméticos, que explicarían las psicosis paranoides anfetamínicas.
Las sustancias psicotomiméticas que se formarían como consecuencia del errado camino metabólico son, entre otras, las siguientes:
– DMPEA (3,4-dimetoxiferriletilamina).
– DMT (N, N-dimetiltriptamina).
– Bufotenina (5-hidroxi-N, N-dimetiltriptamina).
– 3,5 MEO-DMT (5-metoxi-N, N-dimetiltriptamina).
La DMPEA es un derivado dimetilado de la dopamina, cuyos precursores catecolamínicos son los aminoácidos fenilalanina y tirosina. Normalmente, la dopamina se transforma por la acción de la MAO en su metabolito inactivo, el ácido homovanílico. Al disminuir la acción de la MAO, la dimetilación producida por la N-metiltransferasa da origen a este compuesto.
Esta situación puede agravarse por el hecho de que en muchos enfermos esquizofrénicos se halla disminuida la acción de la enzima dopamina-betahidroxilasa, que transforma la dopamina en noradrenalina, aumentando así el nivel de dopamina circulante y, en consecuencia, el de DMPEA.
Los tres restantes compuestos se originan por un error metabólico al disminuir la deaminación oxidativa por falta de actividad de la MO.
Normalmente, los metabolitos del triptófano (triptamina, serotonina y 5metoxitriptamina) son degradados por la NIAO a distintos derivados del ácido indolacético, excretándose de esta manera en forma inactiva.
Si disminuye la actividad de la MAO, esta degradación indólica es suplantada por la transmetilación y se origina así la N, N-dimetiltriptamina (DMT), la bufotenina y la 3,5-metoxidimetiltriptamina (3,5-MEO-DXIT) (30).
La DMT es un derivado dimetilado de la triptamina, que se encuentra en la orina de pacientes esquizofrénicos agudos de forma muy fugaz.
La bufotenina es un derivado dimetilado de la serotonina. Fischer y Spatz encontraron valores de serotonina aumentados en enfermos esquizofrénicos, que disminuían luego del tratamiento con neurolépticos; de ello infirieron que los neurolépticos no sólo bloquean receptores dopaminérgicos sino que impiden también los procesos de transmetilación, disminuyendo así la concentración de sustancias psicotóxicas.
La 3,5-AMO-DMT es un derivado dimetilado de la 5-metoxitriptamina.
Dado que la clozapina regularía el incremento anormal de serotonina, a través del receptor 5-HT2, se estudia la posibilidad de utilizar la determinación de la MAO baja como predictor de buena respuesta a la clozapina en pacientes que presenten altos niveles de compuestos demetilados de la serotonina (como son la dimetiltriptamina y la bufotenina).
La actividad metilante en sangre total (actividad N-metiltransferasa, ANMT) es un procedimiento de utilidad, para certificar el incremento de transmetilación, que presentan este tipo de pacientes. Un aumento de este índice, puede indicar un alta vulnerabilidad clínica en comparación a otros pacientes que no la poseen. Hemos observado en pacientes esquizofrénicos y borderlines que dicho aumento se asocia, ante situaciones estresantes, al recrudecimiento de la patología psicótica (inclusive la aparición de actividad alucinolítica y delirante de comienzo abrupto). De los 18 sujetos que hemos estudiado, 11 presentaron valores altos, encontrándose hasta un incremento 7 veces mayor de la actividad N-metilante, con respecto a la población normal.
Se halló una correlación significativamente negativa, entre los valores de la MAO plasmática y la actividad N-metilante (r= 0.6986; p= 0.001), los pacientes con disminución de la MAO presentan altos valores de la actividad N-metilante. A mayor cantidad de sustrato (serotonina), mayor sería el incremento de actividad metilante, ya que se encuentra directamente asociada al volumen total del sustrato. Se concluye que a mayor serotonina, mayor incremento de la actividad N-metilante.
Es una determinación que se deberá tener en cuenta, dado que un porcentaje de incremento mayor al 10 % de la actividad N-metilante se la puede considerar como un indicador de riesgo para este tipo de pacientes.
Siempre que se presuma la posibilidad de un proceso psicótico enmascarado por un cuadro depresivo, la vía de abordaje psicofarmacológica será en primer lugar la administración de neurolépticos, a modo de pantalla protectora, para recién después indicar el antidepresivo.
Existen antecedentes infantiles y de la adolescencia, respecto del deterioro de la función social e intelectual de la esquizofrenia de tipo II del adulto, revelado por diferentes estudios. Este deterioro premórbido sería un indicador de vulnerabilidad. La misma podría estar determinada, por un proceso de mielinización tardía en la adolescencia y un error de la reestructuración o poda (pruning) sináptica, producida en los últimos años de la niñez y en los primeros de la adolescencia. En estos pacientes adolescentes estaría indicado la determinación de la actividad N-metilante, aún con mayor razón, si existe consumo de marihuana, ya que la misma aumenta 6 veces el riesgo de contraer esquizofrenia y además algunos metabolitos son alucinógenos. La presencia de altos niveles de dimetiltriptamina, bufotenina o un incremento más alto que el 10 % de la ANMT sería un marcador de riesgo de contraer la enfermedad.
Acetilcolina
A este neurotransmisor se lo considera un mediador en los procesos de la memoria y del aprendizaje en el sistema nervioso central.
A nivel periférico presenta dos acciones:
a) acción nicotínica, estimulante de los ganglios autónomos y el músculo estriado, y
b) acción muscarínica, estimulante de las secreciones glandulares y el músculo liso. Estas acciones no tienen un total correlato a nivel del sistema nervioso central.
El segundo mensajero en este caso sería la guanosina-monofosfato cíclico, similar al AMP cíclico.
La acetilcolina es rápidamente degradada por la enzima colinesterasa presente en la circulación y en los tejidos periféricos.
La nicotina se comporta como estimulante en dosis bajas, mientras que en dosis altas produce bloqueo del receptor con aumento de la sedación.
Los receptores muscarínicos pueden ser de dos tipos, MI o M2. El primero está relacionado con la secreción gástrica y la estimulación de los ganglios simpáticos, y el segundo con los efectos de regulación sobre el sistema nervioso autónomo.
Histamina
Se creyó que tenía importancia desde el punto de vista psiquiátrico cuando se descubrió que pacientes esquizofrénicos presentaban altos niveles de histamina circulante. Sin embargo, lo único que pudo comprobarse es la hiperreactividad a la histamina que presentan estos pacientes. Su metabolito periférico, el ácido imidazolacético, está también elevado en la enfermedad esquizofrénica.
Puede activar la adenilciclasa y aumentar el AMP cíclico. La histamina y la serotonina se denominan autacoids para señalar su carácter de hormonas locales, ya que el término hormona da a entender acciones a distancia.
Existen dos receptores diferentes para la histamina: HI y H2. El HI se caracteriza por producir vasodilatación, broncoconstricción y espasmos gastrointestinales, y es bloqueado por los antihistamínicos clásicos. La prometazina es un neuroléptico y potente bloqueador del receptor H l. El receptor H2 produce aumento de la secreción gástrica y es bloqueado por la acción de la cimetidina y similares.
Ácido gammaaminobutírico (GABA)
Se pudo comprobar que este neurotransmisor aumenta cuando se administran barbitúricos y benzodiazepinas. Se caracteriza por estimular los procesos de inhibición neuronal en todas las áreas del sistema nervioso central. La acción anticonvulsivante y miorrelajante se debe a un aumento de la inhibición que provoca este neurotransmisor sobre otras células neuronales. Impide el incremento de la excitación neuronal por aumento de la permeabilidad a los iones de cloruro cargados negativamente.
Las neuronas gabaérgicas se encuentran en la glia, en la hipófisis anterior, en el hipotálamo y en las células beta de los islotes pancreáticos.
Si bien es un neurotransmisor inhibitorio, muchas células gabaérgicas se encuentran inhibidas por otras similares; fármacos como las benzodiazepinas o el ácido valproico, al estimular el GABA, pueden aumentar la inhibición («feedback negativo») y disminuir la inhibición de otras interneuronas con la consiguiente activación paradójica.
Existen dos tipos de receptores gabaérgicos: uno que se caracteriza por actuar sobre los canales de cloro (ionóforo de cloro, GABA-A) y otro que lo hace sobre los de calcio (GABA-B). Las benzodiazepinas actúan sobre el GABA-A. Las beta-carbolinas pueden bloquear estos efectos, produciendo convulsiones y ansiedad.
Se forma a partir de la glucosa que origina ácido glutámico. La enzima glutámico-decarboxilasa (GAD) lo transforma en GABA, que es destruido por la gabaaminotransferasa (GABA-T) en ácido succínico. La GAD está en interneuronas, riñón, hígado, páncreas, ganglios autónomos, epífisis e hipófisis posterior. La GABA-T tiene una distribución similar a la de la MAO: mitocondrias, médula espinal, nervios craneales, cerebelo, células de la glia y células ependimarias productoras de líquido cefalorraquídeo.
Aumenta el turn-over de acetilcolina, disminuye la prolactina y el factor liberador de corticotrofina, y aumenta la hormona de crecimiento.
En la corea de Huntington existe una degeneración de las neuronas gabaminérgicas de los núcleos de la base, lo que ocasiona la producción de agitados movimientos irregulares, que sólo al comienzo de la enfermedad pueden reprimirse voluntariamente.
Su administración por vía oral o parenteral es ineficaz, ya que no se une a las proteínas ni puede pasar la barrera hematoencefálica.
Aminoácidos excitatorios: glutamato y aspartato
El glutamato es la forma aniónica del ácido glutámico y con el aspartato constituyen los denominados aminoácidos excitatorios (EAA).
Tienen tres tipos de vías:
a) las que parten de la corteza y se dirigen al estriado y al hipocampo (en especial receptores no-NMDA),
b) las del bulbo olfatorio que se dirigen a la corteza piriforme, tubérculos olfatorios y amígdala, y
c) los circuitos neuronales situados en el tubérculo cuadrigémino superior y en el cerebelo.
Están involucrados en la memoria, la isquemia y las crisis de epilepsia.
Se sintetiza a partir de la glutamina alimenticia a través de la glutaminasintetasa y puede convertirse en GABA (neurotransmisor inhibitorio) por la glutámico-decarboxilasas.
El ingreso del calcio a la neurona postsináptica y la liberación retrógrada del óxido nítrico realimenta la síntesis del glutamato y es la base de la coactivación de dos neuronas, base para el almacenamiento de la memoria de largo plazo (ver también cap. 13).
El fenómeno «del restaurante chino», producido por la ingesta copiosa de glutamatos, produce sensación de opresión en la nuca y el tórax, cefaleas, náuseas y dolores abdominales; puede llegar a crisis epilépticas.
El glutamato una vez liberado a la sinapsis puede unirse a los receptores NMetil-D-Aspartato (NMDA) o a los no-NMDA; puede se recaptado por la glia para se almacenado en las mitocondrias donde integrar el ciclo de Krebs como base energética o puede recaptarse de forma presináptica ligado a los canales iónicos por las neuronas (en especial del hipocampo) y por los astrocitos de la glia.
Existen diferentes tipos de receptores:
a) ligados a canales iónicos, intervienen en los procesos de memoria a través de la potenciación de largo plazo (long term potentiation, LTP), en las neuronas del hipocampo:
– N-Metil-D-Aspartalo, NMDA (5 subtipos): poseen una alta permeabilidad a la entrada de sodio y calcio, puede ser bloqueado por el magnesio;
– no NMDA: quiscalato, kainato y AMPA (alfa amino 3- hidroxi, 5-metil, 4-isoxasol propiónico). El AMPA presenta dos subtipos uno rápido (que potencia la estimulación) y otro lento, ambos regulan la entrada del sodio y la salida del potasio. El aniracetam, retarda el cierre del canal iónico, del receptor AMPA (ver cap. 16).
b) metabolotrópicos:
– se activa por el glutanmato y depende de las oscilaciones del cloro. Actúa por el sistema de segundos mensajeros: formación de inositol trifosfato (IP3), e inhibe la adenilcicalsa y el AMP cíclico. El almacenamiento el glutamato en las vesículas sinápticas depende de una bomba ATPasa
Los bloqueadores no competitivos más conocidos son los anestésicos ketamina y fenilciclidina (PCP) y actualmente la memantina (ver cap. 16), se la utiliza como neuroprotector. La PCP es una droga adictiva que puede provocar la aparición de síntomas psicóticos y exacerbar los de la esquizofrenia.
Se lo considera asociado a la memoria y a la hipoxia. La estimulación del receptor NMDA provoca el ingreso de iones cálcicos en la neurona con el peligro de muerte celular. El magnesio y el MK-801 pueden bloquear esta acción. No se debe olvidar que el ácido caínico se utiliza en farmacología experimental como destructor del soma neuronal.
El ácido caínico y el glutamato en dosis altas pueden provocar la muerte neuronal en regiones circunscriptas. Por ejemplo, la esclerosis lateral amiótrofica se la trata con antagonistas glutamatérgicos.
Taurina
Es un ácido sulfónico producido por la hidrólisis del ácido taurocólico de la bilis; es un aminoácido inhibidor. Se la relaciona con propiedades antiepilépticas.
Adenosina
La adenosina es un nuclesósido formado por un azúcar (la ribosa) en combinación con una base purínica (la adenina). Puede ligarse a una, dos o tres uniones fosfóricas (AMP, ADP, ATP). La degradación del ADN y ARN producen este nucleósido cuya catabolismo forma las xantina, que se excreta como ácido úrico.. Ver el cuadro 16:
Se caracteriza por ser un modulador de la entrada citotóxica del calcio a la neurona. Dado que es un metabolito del ATP que puede ser liberada por cualquier neurona y ser captada por las neuronas y la glia por su receptores específicos.
Al activar los canales de potasio y cloro, impide la despolarización excesiva que realiza el calcio, a través de los aminoácidos excitatorios (NMDA). Ello se nota, en especial, en los traumatismos craneanos e insuficiencias vasculares que producen alteraciones degenerativas. Ése es el motivo por lo que se lo considera un neuroprotector.
Los astrocitos que mantienen una recaptación permanente de potasio y de aminácidos excitatorios (glutamato) impiden una despolarización neuronal excesiva con el peligro, por ejemplo, de generar convulsiones.
Se conocen diferentes tipos de receptores:
A1: se localiza pre y postsinápticamente, es mediado por la proteína G de manera inhibitoria ya que bloquea a la adenilciclasa, que es la enzima generadora de AMP cíclico. Posee efectos centrales analgésicos, sedativos, anticonvulsivantes y ansiolíticos.
A2a: localizado en zona donde existe la dopamina (estriado y putamen).
A2b: de menor afinidad por la adenosina, se lo compara con el A3. Participa de la regulación de la interleuquina-6 en el astrocitoma.
A3: necesita de altas concentraciones de adenosina para ser estimulado.
Todos los bloqueantes de adenosina Al empeoran los procesos isquémicos en tanto que los agonistas los mejoran (neuroprotectores) (ver cap. 16).
Las bloqueantes de adenosina más conocidos son las formaciones que constituyen las aminopurinas y las metilpurinas. Las más conocidas son cafeína, teobromina y teofilina, que son antagonistas de los receptores adenosínicos, y que poseen propiedades estimulantes a nivel central. Existen estudios con agonistas de la adenosina como la propentoxifilina (que actúa como antifósfodiesterasa), que estimula al ARN mensajero a la producción de factores neurotróficos.
Las benzodiazepinas poseen efectos sinérgicos con la adenosina.
1-15. Neuromoduladores
Los neuromoduladores se caracterizan por atenuar o amplificar las señales sobre grupos neuronales.
Las prostaglandinas son ácidos grasos, que existen normalmente unidos a las membranas celulares, de casi todas las células del organismo. Para su liberación, es necesaria la acción de una fosfolipasa que se activa por influencias humorales, hormonales y nerviosas.
Se conocen numerosos tipos de prostaglandinas (A, B, C, etc.) que actúan sobre diferentes órganos efectores (útero, pulmón, etc.).
La prostaglandina E, aislada de las terminaciones nerviosas, inhibe la liberación de noradrenalina y facilita la aferencia de estímulos dolorosos. Dado que no puede ser inactivada rápidamente por el sistema nervioso, su rol sería el de modulador. Su acción es antagonizada por la aspirina y otros analgésicos. Su liberación es favorecida por la morfina y sustancias de tipo tiramínico o feniletilamínico (queso, alcohol, chocolate, etc.).
Los fosfolípidos, a través de la fosfolipasa (PLA-A 2), forman el ácido araquidiónico, que genera las prostaglandinas. Éstas actuarían como receptores de membranas, en la transmisión intermembrana y como segundos mensajeros.
Características de diferentes receptores
(receptor = proteína que reconoce al neurotransmisor)
1-16. Inmunoneuropéptidos
Comunicación bidireccional:
Las inmunoneuropéptidos y hormonas son transmisores (ligandos) que actúan a distancia: las células inductoras que las secretan no se hallan en contacto directo con las células inducidas o blanco que las reciben. Se clasifican de acuerdo a su origen, tipo de acción y peso molecular.
Se conoce que varios tipos de neuropéptidos son producidos por las células del sistema inmune. Se han reportado sustancia P, calcitonina, colecistoquinina, neurotensina, prolactina, melatonina, directamente relacionadas con linfocitos y fundamentalmente con la acción de las células natural killers (NK), los linfocitos B y T, macrófagos y neutrófilos. Actualmente, el término neuropéptido ha caído en desuso y se lo ha reemplazado por el de inmunoneuropéptidos.
Las células inductoras pueden producir ligandos que actúen sobre células blanco o «target»:
– a distancia: inmunoneuropéptidos y hormonas (secreción hormonal),
– en las cercanías: inmunoneuropéptidos y hormonas (secreción paracrina)
– sobre la misma célula: inmunoneuropéptidos (secreción autocrina).
Existen péptidos y hormonas que se sintetizan en diferentes regiones del hipotálamo (Iímbico, endocrino y posterior), para lograr la estimulación de la hipófisis anterior o posterior cuya secreción liberará las hormonas de los órganos efectores periféricos (ver cap. 2).
Proceso de proliferación
Pueden existir migraciones neuronales inadecuadas de origen virósico: es una de las hipótesis a la que se atribuye la etiología de la esquizofrenia.
El proceso de proliferación normal ocurre cuando las células matrices (matrix cells) se distribuyen selectivamente, permitiendo alcanzar a las células posteriores, el destino biológico apropiado de acuerdo a los factores estructural, codificacional y funcional.
De esta forma, las células matrices contienen el mapa genético, por donde deberán desplazarse las células venideras de acuerdo a su tipo celular. Las células matrices son altamente sensibles a diferentes noxas teratogénicas, como por ejemplo son la hipotermia, los metales, los fármacos, la hipoxia, la desnutrición y las radiaciones.
Existen inductores de proliferación celular paracrinos (se secretan en células vecinas) y endocrinos (se secretan en células a distancia), que actúan por intermedio de receptores citoplasmáticos:
– Las somatomedina secreta en el hepatocito como respuesta a la hormona de crecimiento. Estimula la proliferación cartilaginosa.
– El factor de crecimiento nervioso (NFG) se secreta de forma paracrina.
Tener en cuenta este proceso de vulnerabilidad de las células matrices es de fundamental importancia para la psicofarmacología clínica, ya que las acciones de un fármaco, o la asociación de diferentes moléculas, podrían producir alteraciones reversibles o irreversibles.
Si se altera el mapa, se producirá una alteración de la migración celular; es decir, células con una tipología de unidad A arribarán a una zona prevista para células de unidad B. Este atipismo citoarquitectónico, podría producir daños inmediatos o detectables recién en la pubertad, precisamente, cuando los mecanismos de autonomía del yo, requieran de la más absoluta disponibilidad cerebral, para hacer frente a las crecientes exigencias del medio.
Por ejemplo una de las teorías de la etiología de la esquizofrenia, es la que atribuye la enfermedad a una migración anormal de células especializadas hacia la corteza entorrinal, produciéndose un disbalance celular entre corteza entorrinal y área córtico-subcortical.
Los psicofármacos podrían alterar la vida intrauterina, como lo demuestran los cambios en la conductibilidad nerviosa, en la alteración de la afinidad y especificidad de los receptores (de cerebro y placenta) y en la disminución de la concentración de mielina (con la alteración del proceso de mielinización, que afectaría la velocidad de conducción nerviosa).
La exposición materna al virus de la influenza en el año 1955 aumentó el porcentaje de esquizofrenia. El 80 % de las madres de hijos esquizofrénicos estuvieron expuestas al virus de la influenza. En la actualidad se identificó a los virus que dependen del sistema de comunicación bidireccional (inmunoneurobiológico), y que
pueden afectar la migración celular, debido a un cambio del mapa genético de las células matrices.
También otras noxas pueden alimentar el porcentaje de la esquizofrenia: infecciones dermatológicas simples, tratadas inadecuadamente puede inducir en la progenie, un aumento del porcentaje de esquizofrenia y una aberración dermatológica en manos y en pies; el uso perinatal de aspirina alimenta el riesgo de esquizofrenia presumiblemente por modificaciones del flujo en diferentes regiones cerebrales; la infección virósica del trigémino asciende por vía trigeminal al temporal medio y de allí al cerebro límbico, produciendo síntomas psicóticos a veces de carácter irreversible (la distancia entre la mucosa nasal al córtex temporal es de sólo 15 mm).
1-17. Apoptosis y necrobiosis patológica
La muerte celular programada (apoptosis) se produce por activación genética, al cesar la producción de factores tróficos de células vecinas y la apoptosis aberrante por una falla genética en algunas células.
Normalmente, existe una muerte celular programada genéticamente (apoptosis), que se produce al faltar factores proteicos tróficos de origen paracrino. Se activa la fosfolipasa C, que a través del IP3 produce aumento de calcio y de endonucleasas, que fragmentan al ADN, desarma el citoesqueleto, compacta la cromatina, produce vesículas apoptósicas, que finalmente son digeridas por macrófagos.
La alteración del código proteico en macrófagos se puede producir por una alteración, por ejemplo viral: si se altera la proteína GP-120-macrófago, se produce una aberración en el programa de poda celular de sinapsis o neuronas redundantes o aberrantes debido al cambio del «blueprint» de la información del macrófago y su acción (esta necrobiosis es una apoptosis patológica). El resultado final de esta apoptosis y necrobiosis es que los macrófagos no discriminan entre células vivas (células con adecuación neuroespecífica) de células redundantes o muertas. Sin embargo, factores exógenos o endógenos pueden inducir una falla genética en los macrófagos produciendo una fagocitación aberrante. Un ejemplo de ello podría ser la alteración genética de los macrófagos, que produce una modificación en la lámina medular superior del girus hipocampal que ocasionaría la producción de síntomas esquizofrénicos.
Otra manera de alterar el código genético son los cambios que puede sufrir la región del ADN, llamada el complejo mayor de histocompatibilidad, que son proteínas que marcan a las células de tal manera como para poder reconocerlas de las extrañas. Al no poder diferenciarlas (ya sea por alteraciones genéticas o por otro tipo de noxas) se genera la autodestrucción celular como, por ejemplo, son las enfermedades autoinmunes (lupus, tiroiditis, etc.).
1-18. Psiconeurobiología de las acciones terapéuticas y efectos secundarios
La eficacia y la mayor amplitud en el rango de respuesta de un psicofármaco, no teniendo en cuenta aquí los factores inespecíficos, dependen de las siguientes acciones biomoleculares:
1) Elección adecuada de la molécula.
2) Dosis suficiente.
3) Tiempo suficiente.
4) Asociación adecuada.
5) Previsión de la interacción molecular con otras drogas.
6) Previsión de efectos secundarios.
7) Estratificación del grupo etario al que se le administra el psicofármaco (edad, estado clínico, tipo de respuesta a tratamientos anteriores).
8) Exotoxicosis (evaluación de consumo de sustancias: alcohol, cocaína, marihuana, ácidos, opioides, etc.; como así también: té, café, bebidas de tipo colas, cigarrillos).
9) Dosificación diaria (cuanta menos dosis mejor), y
10) Estrategia de potenciación.
1-19. Eficacia psicofarmacológica según la regulación de la expresión genética
La duración de los efectos psicofarmacológicos de largo plazo, dependen del neuroaprendizaje, de la neuroplasticidad y de la transcripción genética celular, que haya logrado realizar la neurona.
Para que no cese la acción terapéutica de un psicofármaco, un vez que se suspende su administración, tiene que haber logrado interdigitar una estimulación persistente, llamada «full blond», de manera tal de haber generado sucesivamente
a) un «efecto de memoria» o neuroaprendizaje,
b) una «transcripción genética», y
c) una «neuroplasticidad».
De esta forma, la célula «aprendió» un nuevo mensaje, que fue introducido por un ligando exógeno.
Neuroaprendizaje
Los cambios en la conducta se atribuyen a las modificaciones de largo plazo mediados por la potenciación a largo plazo y la transcripción genética.
Un estímulo externo o interno, ya sea provocado por factores ambientales (estrés) o por un psicofármaco, produce sobre la neurona un quantum de energía que se transforma en información. La misma puede, según su persistencia y su codificación química, alterar en forma transitoria o permanente el funcionamiento celular.
La memoria celular es una característica por la cual la célula no puede convertirse en otro tipo celular. Las neuronas como no se dividen permanecen así hasta su muerte biológica. Pero, a través de los cambios en la síntesis de proteínas pueden acumular memoria y nuevos aprendizajes en el cerebro.
Los estímulos agudos, pero de corto plazo, tienden a producir modificaciones de carácter cuantitativo. Es decir, podrán aumentar o disminuir la densidad de los sitios de receptores, y por medio de fosforilaciones proteicas actuar sobre la memoria a corto plazo.
En cambio los estímulos de largo plazo, tienden a producir cambios estructurales ya que modificarán el código de transcripción genética y permitirán mantener la memoria a largo plazo a través de la modificación proteica permanente.
Uno de los mecanismos conocidos de neuroaprendizaje, a través de la investigación de invertebrados, es la potenciación de largo plazo (LTP, long term potentiation).
La LTP consiste en un aumento de las respuestas postsinápticas, luego de estimulaciones presinápticas continuas. Es necesaria una estimulación sostenida: debe ser breve (menor a un segundo), pero de frecuencia elevada (superior 100 Hz). Para representar este nivel de intensidad se la podría equiparar al funcionamiento de un motor a 6.000 revoluciones por minuto, pero en el término de un segundo.
Este mecanismo es importante para la fijación de los engramas mnésicos a largo plazo. Los engramas son los cambios neuronales que se producen durante el proceso de fijación de la memoria (considerada como tal al registro, fijación y consolidación de una conducta aprendida).
El LTP es un mecanismo de potenciación de la memoria para su almacenamiento y depósito. Este refuerzo de la acción entre neuronas pre y postsinápticas es el soporte necesario para la función mnésica. La coactivación de dos neuronas en la sinapsis (de manera que la actividad de una se transfiera a otra) constituye la base de la eficacia sináptica para el recuerdo y la neuroplasticidad neuronal.
Es necesario, a nivel postsináptico, la activación de los receptores N-Metil-D-Aspartato (NMDA) -que por vía glutamatérgica activan los canales iónicos y permiten la entrada del calcio- y, a nivel presináptico el aumento del glutamato. Luego continuará la cadena de fijación, a través la activación de las proteinoquinasas y calmodulina-Ca dependientes.
Se demostró que el LTP, existe en el hipocampo y se caracteriza por la facilitación sináptica. La destrucción del hipocampo produce amnesia, con pérdida de la memoria de lo ocurrido en las últimas semanas y la imposibilidad para incorporar las nuevas adquisiciones de memoria a largo plazo. Necesita de la integridad de los circuitos emotivos (límbicos), ya que se recuerda lo que se fija con bases emocionales.
Por lo tanto deberá existir un sistema de señales retrógrado neuronal de estimulación presináptica, que difunda desde la postsinapsis. Se atribuye esta acción al óxido nítrico (NO), que se genera a partir de la óxido-nítrico-sintetasa y es recaptada por la terminal presináptica. El óxido nítrico estimula la guanilato-ciclasa que convierte el GTP en GMP cíclico. También estaría implicado es este mismo proceso el ácido araquidónico.
Esta potenciación requiere la síntesis de nuevas proteínas, de manera continua que dependen, a su vez, de la transcripción genética.
Un dato muy importante para la psicofarmacología es que el ADN, que contiene el blueprint celular, no sólo permite la transmisión de la información de una a otra generación, sino que también es función del ADN, reponer la información dentro de la célula requerida, manteniendo entonces, un estado de neuroaprendizaje y neuroplasticidad.
Transcripción genética
El proceso de transcripción consiste en la síntesis de ARN, a partir de los moldes del ADN y el proceso de traducción en la síntesis proteica a partir del ARN transcripto mensajero.
El material hereditario se encuentra en los cromosomas, donde existe el ácido desoxirribonucleico (ADN), que contiene toda la información genética. Se encuentra en el núcleo y las mitocondrias. El ADN está formado por una larguísima cadena de nucleótidos constituidos a partir de un azúcar (pentosa), una de las cuatro bases (pirimídicas o purínicas), unidas por fosfatos de alta energía.
Se considera al cromosoma un texto escrito con un alfabeto de cuatro letras y los nucleótidos serían como los números del 0 al 9, utilizados para los registros telefónicos. La múltiple variación de los dígitos, encierra las diferencias de los mensajes a transcribir, un segmento escrito para esta forma de transmisión se lo llama gen. La función de esta transmisión en la fabricación (síntesis) de proteínas, que a su vez están formados por la combinación de alrededor de 20 filamentos diferentes llamados aminoácidos.
El orden de los nucleótidos del ADN en un gen determina la secuencia de los aminoácidos en la proteína, codificada por ese gen en particular. Cambios, pérdidas, errores o añadiduras en la transcripción de los nucleótidos, en un segmento del ADN, pueden cambiar la función del gen y transmitir esta falsa información a la descendencia: esto se llama mutación.
La energía que utilizan todas la células para realizar su trabajo específico es tomada del nucleótido adenosín trifosfato (ATP), que almacena la energía «cargada», que al liberar energía (el fosfato) se «descarga» y se convierte en adenosindifosfato (ADP). El ATP es producido en las mitocondrias, consiguiendo de esta forma almacenar gran cantidad de energía en un espacio sumamente reducido (cuadro 16).
Los alimentos, degradados por enzimas son oxidados en las mitocondrias para obtener esa energía. Las mitocondrias, que se originaron de bacterias, funcionan simbióticamente con las células humanas. Están controladas por un gen propio de 16.000 nucléotidos que se transmite por vía materna. La decarboxilación oxidativa, el ciclo de Krebs y la fosforilación oxidativa que se lleva a cabo en esta fábrica de energía mitocondrial, libera anhídrido carbónico y agua sólo en presencia del oxígeno, que le llega por vía aeróbica.
La fosforilación oxidativa, como se verá más adelante, es la vía más importante para la acción psicofarmacológica a largo plazo mediado por este tipo de transcripción genética.
La información codificada en el ADN tiene los siguientes elementos: dos cadenas polinucleótidas; una azúcar, desoxirribosa; bases nitrogenadas pirimídicas, la citosina y la timina; bases purínicas, adenina y guanina; uniones fosfóricas; y una enzima hidrolítica, la desoxirribonucleasa.
En cambio, la información que codifica el ARN se diferencia del ADN en que tiene una sola cadena polinucléotida; otro azúcar, la ribosa; bases pirimídicas diferentes, citosina y uracilo en lugar de citosina y timina; y enzimas polimerasas, en lugar de las desoxirribonucleasas (ver cuadro).
A través de estos nucleótidos, el ADN tiene la secuencia de la información genética. Esta información es «migrada o transcripta » al ARN, dentro de un proceso conocido como transcripción nuclear (ARN mensajero, ARNm). Ello tiene como objetivo, a través de la codificación de los nucleótidos, la síntesis de determinados aminoácidos y finalmente la síntesis proteica (traducción).
El proceso de traducción se realiza en una parte del citoplasma (citosol).
Por ejemplo, una secuencia de nucleótidos, que podría ser C-A-T-C-T-C, puede quedar convertida en tina secuencia C-T-A-G-T-C, y si bien se están usando la misma cantidad de celdas y el mismo tipo de nucleótidos, al cambiar la combinación, se modificará el código genético que luego el ARN a través de su brazo mensajero y su brazo transcriptor, enviará a la proteína,
Existen tres clases de ARN:
a) mensajero (ARNm): lleva la secuencia proteica, tomada del ADN nuclear;
b) ribosómico (ARNr): une los aminoácidos en secuencias determinadas para formar las proteínas;
c) de transferencia (ARNt): transporta y adapta la secuencia del ARN en el ribosoma.
El gen tiene diferentes unidades: el «promotor», que indica a partir de que nucleótido se debe iniciar la transcripción y las «secuencias reguladoras y de terminación», que señalan a partir de dónde se deben hacer los cortes de copia. El ADN ha resuelto codificar la secuencia de aminoácidos sólo en tres tripletes de su base llamado codones.
Existen secuencias de nucleótidos totalmente utilizables para el ARNm (exones), y nucleótidos de secuencias superfluas (intrones), que serán eliminadas del ARN, al salir de núcleo celular. De esta manera la secuencia del ARN, será totalmente utilizable. Este proceso produce una migración informativa hacia las proteínas y cambio de la expresión genética de la célula (proceso de traducción).
Para este proceso es necesaria la participación de los llamados factores de transcripción (FT). Éstos son proteínas complejas capaces de activar al «promotor» y su secuencia nucléotida.
El promotor tiene 2 secuencias de nucleótidos: «TATA (timina-adeninatimina-adenina) y CAAT (citosina-adenina-adenina-timina). Estas secuencias de nucleótidos se encuentran a 25 bases, corriente abajo, del sitio de transcripción y juntamente con los factores de transcripción y las polimerasas 1 y 11 son las responsables de la transcripción genética.
El proceso se inicia cuando el Factor de Transcripción IID, por medio de la Tata Binding Protein (TBP) altera la cromatina en el promotor, que de la forma rectilínea pasa a tener un ángulo de 100′, lo que provoca la atracción de las ARN-polimerasa II. Esta polimerasa se fosforila, por la donación que recibe de fosfatos desde el ATP, y provoca la apertura de la doble hélice del ADN, señal de comienzo de la síntesis del ARNm.
1-20. Protoncogenes
Son considerados genes que pueden ser modificados por los neurotransmisores.
Sin embargo, dentro del proceso de transcripción existen factores de represión o de rechazo de la nueva información llamadas proteínas represoras. La secuencia de transcripción puede interrumpirse por la acción de estas proteínas represoras que pueden ser de diferentes tipos:
– tipo A: genes inmediatos (Inmediate Early Genes, IGEs), y
– tipo B: proteínas transcriptoras «cis».
Se los llama genes inmediatos, porque su transcripción puede ser activada inmediatamente y de manera transitoria sin necesidad de la síntesis de nuevas proteínas. Incluye las familias fos, jun y zif 268. Dado que estas familias de genes se las encontró en virus se las diferenció de ellos adicionando la letra c en lugar de la v: c-fos y c-jun en lugar del tipo virósico denominado v-fos y v-jun. En el cerebro, se encuentran el c-fos y el c-jun, que inducirían cambios en la regulación sináptica.
Se lo llamó c-fos como siguiente en la lista de los sarcomas osteogénicos FBJ y FBR. Codifica fosfoproteínas nucleares que modulan a otros genes. Responde a estímulos como son los neurotransmisores y a diversos factores de crecimiento. Es considerado un tercer mensajero en el sistema de transducción celular.
El c-jun, llamado así por un investigador japonés, que lo descubrió y abrevió el nº 17 en japonés (ju-nana), que correspondió al orden numérico, sobre otros 30 oncogenes inductores de sarcomas en pollos. El c-jun se liga al factor de transcripción proteico A-P-1, encargado de transmitir información celular a través de las proteinoquinasas y al c-fos lo que les permite a ambos incrementar el control sobre otros genes actuando ambos como «terceros mensajeros».
A estas formas se las denomina habitualmente protooncogenes, ya que la mutación de los mismos en seres humanos produce un aumento de proliferación de células cancerosas (oncogenes). Sólo en especies avícolas se demostró el desarrollo de cáncer a partir de la inyección de protoncogenes virósicos (sarcoma de pollos).
Por ejemplo, un protooncogen fos combinado con la acción del ARN mensajero es traslocado y transformado intracitoplasmáticamente, donde el producto de su forma proteica (Fos) inicia una serie de operaciones tendientes a la modificación de la expresión genética. En este proceso, el Fos (derivado proteico del oncogén fos), una vez dentro del núcleo celular y con la participación de Jun (factor de transcripción), se ligaría a sitios de regiones genéticas, en determinadas partes de la secuencia del «promotor» iniciando de esta forma la regulación, relacionada con la modificación de procesos que incluyen a segundos y terceros mensajeros. Por ejemplo los genes de las proencefalinas y los de la tirosina-hidroxilasa.
Los protooncogenes codifican numerosas proteínas: factores de crecimiento, el receptor citosólico de la hormona tiroidea, proteínas nucleares, etc. La proteínas formadas por los protooncogenes se las designa con la primera letra en mayúscula: Fos y Jun.
El fos ARN mensajero es translocado en el citoplasma para la producción de la proteína Fos, para pasar luego nuevamente al núcleo y ligarse junto con el Jun.
La despolarización neuronal (glutamatos, TEC por ejemplo) o la actividad de ciertos psicofármacos induce la formación de Fos, en ciertas regiones cerebrales (tálamo, áreas sensitivo-corticales).
El c-fos y el c-jun son generalmente activadores de la transcripción, pero dentro de los miembros de la familia Fos, se encuentran los C-Fos/jun-B, que contienen Fos tipo B y que pueden reprimir la transcripción.
Algunos genes contienen elementos cis-reguladores, que se ligan a la proteínas represoras de la transcripción. A diferencia de los elementos trans (factores de transcripción), que pueden estar en cualquier lugar del genoma, la presencia de elementos cis, en una determinada célula, bloquea la expresión genética de todos esos genes para ese grupo celular.
Los cis son proteínas especializadas, que forman parte de los sitios de ligaduras, dentro de los genes, para que se genere la transcripción. La afinidad de la unión no siempre será positiva, pudiendo esta proteína reprimir el mensaje, y rechazar el intento de transcripción.
Su calidad de represión podrá ser benigna o maligna, ya que si el estímulo es la transcripción de un atipismo celular -generador de una enfermedad oncológica o de carácter viral-, la represión será de carácter benigno, pues estará al servicio de la resistencia y de la defensa del anteproyecto celular o blueprint.
Una vez que las polimerasas tipo II activan los factores de transcripción (TF), pueden ocasionar los siguientes cambios de señales, que actúan a nivel celular:
a) corrección de lo que la célula hace mal (efecto de las drogas terapéuticas);
b) funcionamiento de manera equivocada o aberrante (efecto por alteración viral, depresiones, estados de sobreexcitación, por abuso de sustancias, etc.);
c) modificación del blueprint, alterando el genotipo y el fenotipo, produciéndose un atipismo (células tumorales).
Es muy importante conservar lo más intacta posible la señal celular, para evitar enfermedades psiquiátricas, para no promover alteraciones génicas que puedan producir: variaciones inmunológicas, afectando a los linfocitos B y a las células T y NK; para evitar variaciones celulares o metabólicas, que tiendan a la proliferación y al desarrollo del factor de proliferación tumoral (TGF), en el paciente oncológico.
Neuroplasticidad
Los neurotransmisores pueden inducir cambios en la habilidad de aprender y adaptarse del cerebro, fundamentalmente, a través de las fosforilaciones proteicas y transcripciones genéticas.
La plasticidad es la capacidad de las células embrionarias primitivas para adecuarse al ambiente inmediato. En relación con la vida adulta, sería la capacidad de reconstrucción de tejidos o de la restauración de su parte perdida.
Sin embargo, sólo las neuronas adquieren un nivel tan desarrollado de bioaprendizaje, diferenciación y complejización de funciones.
La neurorregeneración, el neuroaprendizaje y el neurodesarrollo se concebían, hace muy poco tiempo, hasta la finalización del período evolutivo, luego del cual la neurona se comporta con variaciones cuantitativas, sensible a los cambios de estímulo, pero siempre dentro de un marco de estabilidad, sin que se produzcan cambios de lo aprendido en lo que respecta a la memoria neuroquímica.
La neuroplasticidad sería la capacidad de la neurona de inducir cambios internos, que la llevarían a un proceso de neuroadaptación y neuromodulación, a través del cual podría cambiar o reaprender el tipo de respuestas que brindaría al medio. Este proceso podría ser rápido o de largo plazo, determinado por dos mecanismos:
a. la fosforilación de proteínas, y
b. la regulación transináptica genética.
El bloqueo a largo plazo producido por psicofármacos, que antagonizan a ciertos receptores (por ejemplo, el bloqueo de la dopamina por los antipsicóticos), induciría a la neuroplasticidad.
Esta persistencia de la acción sobre el receptor llevaría, en el largo plazo, a una modificación en la expresión genética.
Estas modificaciones en los cambios de la sensibilidad del receptor, mediadas por el efecto de drogas, podrían servir para explicar sus efectos terapéuticos y colaterales.
También son posibles cambios neurofisiológicos a través de la modificación de la experiencia (estrés, psicoterapias, socioterapias).
En realidad los cambios proteicos producidos por la fosforilación no implican cambios en la síntesis proteica, de allí que se pueden expresar los cambios celulares de manera rápida. Existen receptores de membrana que producen señales intracelulares luego de fosforilarse, ellos son:
1) la tirosinaquinasa: fosforila la tirosina citosólica y aumenta la conversión de tirosina en dopa,
2) la serian terminan: fosforila a serinas y treoninas, y
3) la guanilatociclasa: convierte GTP en GMP cíclico.
Las proteínas fosforiladas alteran rápidamente su carga eléctrica porque los grupos fosfatos están cargados muy negativamente, lo que altera la conformación de la proteína y permite que interactúe con otras moléculas y canales iónicos. Así por ejemplo el receptor beta-adrenérgico disminuye su afinidad por la noradrenalina.
La regulación transináptica genética se hace a través de las proteínas CREB (Cyclic Response Element Binding), consideradas terceros mensajeros, que se ligan a una parte determinada del ADN (llamada elemento AMP, que contiene una determinada secuencia de nucleótidos), y fosforiladas, por proteinoquinasas intranucleares, actúan sobre proteínas del tipo FOS o cuartos mensajeros.
1-21. Resumen
Cuando la ARN-polimerasa se une al «promotor», se fosforila por el factor de transcripción; luego se libera de ellos y permite abrir la doble hélice del «ADN marcado» por el promotor, para iniciar la síntesis del ARN mensajero. La acción de los psicofármacos debe ser de largo plazo para permitir mantener las respuestas conductuales modificadas en el tiempo.
Las acciones psicofarmacológicas deberán relacionarse en el futuro con los siguientes nuevos conceptos:
1) Ingeniería de la expresión genética.
2) Comunicación bidireccional.
3) Comunicación cruzada y de retroalimentación («cross talk y feedback «).
4) Corriente del flujo informativo («information flows»).
5) Anteproyecto celular del ADN («blue print «).
Los segundos mensajeros (AMPc, GMPc, Ca, IP3, DAG) tienen importantes interacciones entre sí («cross talk), ya que ellos son capaces de modificar las proteínas a través de actuar sobre diferentes enzimas intracelulares.
Las funciones más importantes del ADN son las de conservar, retener, proteger y preservar el anteproyecto celular o «blue print «. La estructura del ADN está compuesta por un hélix y dos hebras («stands»). Cada hebra está compuesta por estructuras nucleótidas, en donde se carga la información genética.
La información contenida en el ADN puede ser expresada por el ARN o por proteínas especializadas. La estructura del ADN es rígida, mientras que la estructura del ARN no lo es; por tal motivo, este último es el encargado de la transferencia informativa, ya sea a través de su forma mensajero (m), ribosomal (r) o transferencial (t).
En el proceso normal, el flujo informativo está determinado por la transcripción del ADN hacia el ARN (proceso nuclear), mientras que la traducción está producida por el ARN hacia proteínas especializadas (proceso citosólico). Para que una célula conserve su tipificación, debe conservar su estructura rígida y especializada.
Se pudo demostrar que el estrés, puede producir modificaciones en los protooncogenes y especialmente en el c-fos. Cambios permanentes que induzcan modificaciones en los sistemas noradrenérgicos, dopaminérgicos, acetilcolinérgicos, glutamatérgicos, así como también en la hormona de crecimiento, el calcio, los inmunoneuropéptidos y los glucocorticoides, podrían degenerar el proceso normal de una célula y afectar su tipificación y/o función.
El estrés puede producir alteración del c-fos o del c-jung que tendrían directa repercusión en el flujo informativo, ya sea en el proceso nuclear de la transcripción (ADN a ARNm) o citosólico, de la traducción (síntesis proteica).
Los procesos depresivos graves o las estimulaciones ambientales fuertemente estresoras (procesos de ansiedad generalizada derivados o no de un PTSD), pueden modificar los agentes nucleótidos del strand del ADN o alterar las hélix de azúcares fosfato, modificando y alterando su función del blueprint celular.
Para que las modificaciones del proceso de transcripción del ADN lleguen al ARN es necesario una serie de pasos:
– A través del elemento exon (transcriptor de codificación genética), se induce un cambio de programa en el mensaje del ARN, que transmitirá a través del intron.
– Cuando el intron quede atrapado por una enzima, que le devolverá al ARN su ligadura con el exon, se transcribirá (traducirá) la información a organelas ribosómicas extranucleares, para efectuar la síntesis de la secuencia de amioácidos, que al unirse a través de sus uniones peptídicas, modificarán finalmente las proteínas especializadas, originándose el peligrosísimo cambio de expresión celular.
Este cambio puede ser:
1) Funcional: no determinará que la célula altere el blue print (o sea su anteproyecto original), pero puede, aun conservando su genotipo, comenzar con cambios funcionales.
Si se trata de una célula neuronal, sus efectos clínicos podrían ser: depresión recurrente, ataques de pánico, estados de irritabilidad permanente, inducción a modificaciones inmunológicas.
Si se trata de una célula común, cualquiera de estas modificaciones pueden repercutir tanto en la génesis del cáncer [vía modificación de las células natural killers (NK) o linfocitos TI, como en el paciente oncológico [vía activación indirecta producida por un aumento de los glucocorticoides, alteración en la síntesis de prolactina y melatonina, disminución de la respuesta inmunoantitumoral, afectando directamente el factor de crecimiento tumoral (TGF) ].
2) Definitiva: la alteración en el blue print modifica el fenotipo y genotipo celular. Se puede generar el conocido proceso de atipización celular, asociado a la enfermedad oncológica.
Los estímulos estresantes, los factores tóxicos ambientales, los efectos farmacológicos de algunas drogas, pueden modificar patológicamente a las señales intramembranas protooncogénicas y alterar la funcionalidad o el tipo de las siguientes maneras:
1er. paso: Las acciones farmacológicas y las de los virus; los efectos estresantes y los ambientales alteran los receptores de la post-membrana (modifican su estructura, sensibilidad y mensajes) y al fosfatidilinositol 4,5 fosfato (PIP2), a las fosfolipasas, al diacilglicerol (DAG), a las proteinoquinasas, al calcio intracelular, a la relación calcio-calmodulina y al AMP cíclico.
2do. paso: Afectación de los genes inmediatos (IGE), modificando la cadena de proteínas (la familia c-fos y c-jun), ya modificados por las acciones del primer paso. A partir de aquí se produce la traslocación informativa hacia el núcleo.
3er. paso: Ya dentro del núcleo existen sitios receptores de los factores de transcripción llamados cis. Estos sitios de recepción son activados por los promotores o activadores, que actuarían como mediadores entre los factores de transcripción (oricogenes fos) y los receptores especializados del ADN (receptores cis) .
A partir de aquí, la TATA box, determinada por secuencias de nucleótidos A y T, recibirá el material transcripto y, ya sea a través de proteínas represoras o proteínas activadoras permitirá que ese mensaje ingrese o no a los sitios de ligadura específicos (TATA box binding-protein, TBP) que actúan como proteínas receptoras de nuevos mensajes. Si el mensaje es aceptado, se ponen en marcha polimerasas específicas que finalmente ordenan los cambios en el ARN.
1-22. Tipos de respuesta psicofarmacológica desde el punto de vista genético
El neuroaprendizaje celular en un grupo de pacientes permite que, suspendido el psicofármaco que haya resultado beneficioso, se conserven los cambios positivos de manera definitiva.
Para comprender por qué un psicofármaco produce o no su efecto terapéutico, o para alcanzar una comprensión de por qué existen grupos de sujetos que recaen cuando abandonan el fármaco y otros que no lo hacen (aun cuando luego del tiempo indicado dejen la medicación), es necesario explicar los fenómenos de transcripción y de transformación intracelular.
El tiempo de latencia para que un psicofármaco actúe significa un aprendizaje biológico con un tiempo de espera. Ese tiempo se insume para que la información recibida por el receptor migre a la unidad catalítica, a la proteína G, a los segundos y terceros mensajeros, a los protooncogenes y de allí a los procesos intranucleares. En cambio, si no se logran que estos pasos sean exitosos y existe una «resistencia biológica», no se producirá el efecto del neuroaprendizaje y neuroplasticidad y consecuentemente la acción no se mantendrá en el tiempo.
Se pueden entonces diferenciar cuatro tipos de respuestas farmacológicas:
Tipo I: Responde-Responde (RR)
Es el grupo que tiene resistencia psicofarmacológica absoluta. Desde el punto de vista neurobiológico estos sujetos ni responden ni aprenden.
Tipo II: Responde (R)
Es el grupo que presenta resistencia parcial, es decir, la resistencia puede vencerse aumentando la dosis o con estrategias de potenciación o con la terapia electroconvulsivante. Es decir, que la combinación con fármacos o estrategias de potenciación, pueden sobrepasar la resistencia biológica inicial. Éste sería el clásico ejemplo clínico, en que el paciente sobrelleva un tiempo prolongado sin responder a un psicofármaco y comienza a tener una respuesta 11 cuasi milagrosa» cuando se corrige la dosis, se lo asocia con otro fármaco o se utilizan estrategias de potenciación (ejemplo: se asocia litio a los antidepresivos) .
Tipo III: Responde-no aprende (RNA)
En este grupo de pacientes el efecto terapéutico se mantiene mientras que el sujeto reciba la medicación, ya que si se la suspende, el enfermo recae. En este caso la célula responde al estímulo enviado por el ligando exógeno (psicofármaco), pero no aprende la nueva información porque la transcripción es «reprimida» en alguna fase del proceso.
De esta forma, la neurona necesita recibir permanentemente el estímulo, \u que tiene una incapacidad para el neuroaprendizaje. Una vez que cesa el estimulo, se extingue el efecto terapéutico. Éste es el grupo de pacientes, a quienes es necesario explicarles por qué lo más sensato es administrarles la medicación de por vida: Responde pero no Aprende.
Tipo IV: Responde-aprende (RA)
Es el grupo de pacientes con el tipo de respuesta psicofarmacológica más exitosa. No sólo responde, sino que una vez que pasa un tiempo suficiente asintomático y luego se suspende la medicación, no recaen.
Es el ejemplo de algunos pacientes con ataques de pánico, que luego de un tratamiento psicofarmacológico y psicoterapéutico se consigue producir la remodulación neurobiológica de la hormona liberadora de corticotrofina (CRH), del calcio y de la interleuquina-6, que consigue transcribir la nueva condición intranuclearmente y produce un reaprendizaje neuroquímico y neurobiológico. En este tipo de pacientes el retiro de la medicación no provocará una recaída.
1-23. Efectos secundarios adversos o colaterales
Los efectos secundarios deben evaluarse: con el tratamiento (ecuación riesgo-beneficio psicofarmacológico), con la sensibilidad del paciente (miedos e hipocondría) y con la responsabilidad médica (a través del consentimiento informado, si es necesario).
El reconocimiento de los probables efectos colaterales es tan importante como el conocimiento de la acción terapéutica del medicamento. Habitualmente se trata de efectos nocivos, producidos por dosis terapéuticas, que dependen de la interacción entre el psicofármaco, el enfermo y los mecanismos psicopatológicos que lo aquejan.
Estos efectos adversos son raros y la tasa de morbimortalidad que producen es baja. Los porcentajes de aparición varían de población a población. Así, por ejemplo, en los países anglosajones los analgésicos de tipo pirazolónico presentan un alto porcentaje de agranulocitosis reversible con la supresión del medicamento. Este porcentaje no coincide con el encontrado en poblaciones de origen latino.
Los efectos colaterales, generalmente molestos, pueden incrementar la dependencia del paciente respecto del médico, el psicoterapeuta o la institución que lo trata. Este beneficio secundario de la enfermedad puede ser útil o contraproducente. Lo primero, cuando refuerza el vínculo con el tratamiento hasta la desaparición de los síntomas indeseables. Lo segundo, cuando obliga a los profesionales a realizar un control más intenso del enfermo, a cambiar de psicofármacos de forma constante y a prescribir otros medicamentos que atenúen o impidan los efectos colaterales. Se cae así en un círculo vicioso, muchas veces difícil de romper, hasta que sobreviene el abandono de la medicación, considerada por el paciente como ineficaz y por el médico como perjudicial a causa de sus efectos secundarios.
El médico administrador tendría que evaluar de qué manera comunica al paciente los beneficios y riesgos de la medicación que le será administrada.
El enfermo no está en condiciones anímicas, en numerosas ocasiones, de evaluar lo que significa el hecho de que para aliviar su padecimiento psíquico tenga que aceptar de forma simultánea la probabilidad de que el medicamento pueda provocarle molestias intrascendentes (como, por ejemplo, sequedad bucal en el tratamiento con antidepresivos) y hasta trastornos graves (como son las disquinesias tardías, luego de la administración de neurolépticos). La responsabilidad médica no finaliza al comunicarle o transferirle «todo» lo que el profesional sabe al enfermo. Esa transmisión de la información al paciente oscila desde explicarle el prospecto de envase hasta hacerle firmar un escrito donde manifieste conocer los riesgos de la medicación administrada, tal como se hace en algunos países.
Los efectos adversos se traducen fundamentalmente en el sistema nervioso autónomo, que no se encuentra bajo control voluntario ni consciente (ver cap. 2).
Estos efectos adversos aparecerán de forma más manifiesta y rápida en aquellos pacientes que, en el desarrollo evolutivo de sus emociones y comunicaciones, presentaron fijaciones muy infantiles. Este nivel «visceral infantil» se expresará por una hipersensibilidad de cualquier zona somática donde la medicación ejerza sus efectos farmacológicos. En cambio, aquellos enfermos en quienes la acción, la idea y la expresión se combinen más adecuadamente, mostrarán su hipersensibilidad en esas áreas, con la aparición de una mayor repercusión psicológica de los efectos secundarios.
El miedo del paciente de conectarse con los síntomas que le transmite su cuerpo se intensifica durante la psicofarmacoterapia al no poder disociar («asumir») la mejoría en el área psíquica, de los posibles displaceres momentáneos en áreas somático-viscerales de poco control consciente. Frente al miedo a la muerte repite los síntomas de la enfermedad.
Estos efectos pueden deberse a:
1 ) Intensidad excesiva de un efecto terapéutico. Obtención de una sedación excesiva por administración de ansiolíticos, cuando el efecto buscado era únicamente controlar la ansiedad.
2) Efecto farmacológico inherente al psicofármaco recetado, Los efectos anticolinérgicos que producen los antidepresivos tricíclicos dependen de las características individuales del paciente. Puede presentarse desde una leve sequedad bucal en algunos hasta una retención urinaria aguda y trastornos
cardiológicos en otros.
3) Reacción alégica por hipersensibilidad. Este tipo de reacciones es mediado por
mecanismos de tipo antígeno-anticuerpo. Por ejemplo, reacciones
urticarianas luego de la administración de neurolépticos de tipo fenotiazínico.
4) Reacciones idiosincrásicas. Se deben a mecanismos inmunológicos de origen
genético o constitucional. Por ejemplo, porfiria provocada por la administración de barbitúricos. 5) Interacción con otros medicamentos.
a) Por interferencia entre dos sustancias psicotrópicas: por ejemplo, los barbitúricos aceleran el metabolismo de los tricíclicos. Los antiparkinsonianos disminuyen la concentración sanguínea de la clorpromazina.
b) Potenciación de efectos adversos entre dos psicofármacos: por ejemplo, los efectos colaterales anticolinérgicos de los neurolépticos pueden potenciar los de los antidepresivos.
c) Interferencia de un psicofármaco con otro medicamento: por ejemplo, la administración de antidepresivos tricíclicos antagoniza los efectos antihipertensivos de la guanetidina, y es necesario en estos casos aumentar la dosis del medicamento antihipertensivo. Al suspender la administración del antidepresivo puede producirse una hipotensión, ya que la guanetidina estará con una dosificación alta relativa.
d) Un fármaco no psicotrópico puede interferir en la acción específica de un psicofármaco: por ejemplo, el analgésico butazolidina acelera la metabolización de los antidepresivos tricíclicos. Los diuréticos suelen aumentar la toxicidad del carbonato de litio.
Actualmente la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT), posee un sistema de farmacovigilancia para el registro de efectos adversos, que puede comunicar cualquier profesional a través de un formulario a dicha central. De esta manera sería posible la evaluación estadística, a nivel nacional y con certeza de los efectos secundarios para todo tipo de fármaco.
El profesional es quien deberá evaluar y comunicar los beneficios, riesgos y medidas precautorias de control clínico, de laboratorio y la posibilidad de establecer un consentimiento informado al paciente y/o familiares. Deberá tener en cuenta los síntomas psicopatológicos, los estilos y grado de entendimiento del paciente y su relación con el médico-administrador de psicofármacos v/o clínico.
Este consentimiento, de realizarse por escrito, ya sea en la historia clínica que lleva el médico o en la del establecimiento en caso de internación, deberá especificar, con lenguaje adecuado para el nivel del paciente y familiares, las ventajas y desventajas de los medicamentos a utilizarse, como asimismo los probables y/o posibles efectos secundarios.
En este momento el médico administrador deberá decidir, si es necesario que el paciente y/o familiares firmen el consentimiento, o es suficiente dejar consignado que dicha información fue dada en la presencia de quienes estuvieron en la consulta, aclarando fecha y momento en el que fue realizado, ya que en caso de peritaje caligráfico se puede establecer -con muy buena precisión- la antigüedad del párrafo correspondiente a través del estudio de la tinta y antigüedad del papel de la ficha o historia clínica (ver indicaciones del siguiente cuadro).
Cuadro 18. Características legales del consentimiento informado:
Definición:
«Es una declaración de voluntad de un paciente, que va a ser sometido a un tratamiento que se le propone -como médicamente aconsejable- luego de haber sido adecuadamente informado acerca del mismo y decide prestar su conformidad».
Se debe informar sobre:
1) Naturaleza de la dolencia
2) Características del procedimiento
3) Beneficios
4) Riesgos
5) Alternativas
La pequeña fracción de droga libre unida al receptor es, en definitiva, la responsable de la acción terapéutica. Esta fracción se encuentra en un equilibrio dinámico con los procesos de absorción, distribución, metabolismo y excreción. Cualquier droga que altere alguna de estas fases alterará la fracción libre unida al receptor y, en consecuencia, su acción biológica.
La eliminación de un fármaco que es de naturaleza exponencial se ve alterada cuando existen otras drogas en circulación que actúan sobre los procesos de metabolización y excreción.
Puede ocurrir que algunos medicamentos aumenten y activen el retículo endoplásmico (microsomas) del hígado y provoquen así el incremento en la eliminación de otras drogas. Los barbitúricos, la difenilhidantoína, el alcohol y los hidrocarburos del tabaco producen esta acción con la consiguiente necesidad de aumentar las dosis de los fármacos para lograr los efectos terapéuticos buscados.
Por el contrario, la inhibición de este tipo de metabolismo que produce la clorpromazina, el ácido valproico, la cimetidina y el cloranfenicol, entre otros, provocarán efectos tóxicos cuando se indiquen en dosis convencionales otros medicamentos. Los inhibidores de la MAO tienen esta acción que es usada para obtener efectos terapéuticos útiles.
La lista de las interacciones medicamentosas puede llegar a ser extremadamente larga. El médico deberá tener en cuenta los síntomas de los efectos colaterales e interacciones en una población adulta normal, así como la sugestión a la que están sometidos los pacientes a causa de la información paramédica y de la lectura que hacen ellos mismos del prospecto de envase.
No hay que olvidar que a muchas de las aplicaciones terapéuticas actuales se llegó como consecuencia de la observación de los efectos colaterales que producían ciertos medicamentos. A raíz del uso de los inhibidores de la MAO como drogas antituberculosas, se comprobaron efectos colaterales como euforia y excitación, lo que sirvió para catalogarlos como antidepresivos.
Las propiedades del disulfiram, que lo hacen apto para su empleo en la terapéutica de deshabituación del alcoholismo, fueron descubiertas accidentalmente cuando, usado como antihelmíntico, produjo síntomas de abstinencia alcohólica en un paciente que había ingerido alcohol.
1-24. Valoración de la eficacia de los psicofármacos por escalas de evaluación
Las escalas de evaluación permiten seguir la evolución del tratamiento psicofarmacológico de manera objetiva.
En la actualidad los estudios que se realizan con psicofármacos incluyen diferentes escalas, y la literatura que confeccionan los laboratorios de especialidades medicinales traen esquemas que se basan en los trabajos realizados directamente por el investigador, donde se resalta o recalca la importancia de la acción de la nueva molécula estudiada sobre el placebo u otra ya existente en el mercado,
Es conveniente conocer las escalas, sus ventajas, sus desventajas con sus respectivas puntuaciones a fin de poder aceptar su credibilidad. Su uso, en casi todos los estudios psicofarmacológicos por los investigadores para destacar la eficacia, la ineficacia o los efectos secundarios hace hoy imprescindible el conocimiento de las mismas.
Seria conveniente que el médico administrador intentase puntuar con alguna de ellas sus propios pacientes, con el objetivo de poder tener un criterio de validación individual y de evolución del paciente, como método para poder «creer» de manera científica y no «formal» la propaganda que se hace de los diferentes estudios.
Los factores específicos e inespecíficos hacen difícil la evaluación de los efectos terapéuticos o eficacia clínica de las sustancias psicotrópicas en los seres humanos.
En muchas áreas de la farmacología es posible establecer una relación directa entre los resultados de la experimentación en el campo animal y la predicción de los efectos farmacológicos de las drogas en seres humanos. Este resultado es difícil de lograr en psicofarmacología, ya que no hay en el reino animal equivalentes satisfactorios para producir enfermedades mentales, como la esquizofrenia o la depresión. Sólo es posible determinar la eficacia de un psicofármaco si se lo administra a quien padece la enfermedad.
Lamentablemente, se debe reconocer que para la evaluación clínica masiva de psicofármacos no se posee otro recurso que las escalas de clasificación médica (rating scales) estandarizadas (realizadas por el médico durante la entrevista) y las escalas de autoinforme o autoevaluación (realizadas por el mismo paciente en el transcurso de la consulta).
Escala de impresión clínica global para la evaluación de los resultados (Clinical Global Impression, CGI)
Es una escala muy difundida para la evaluación general de cualquier estudio clínico. Sus ventajas son la rápida visualización en cuatro ejes, con una puntuación especifica, de fácil interpretación, relacionando la eficacia con el efecto adverso. Los ejes son los siguientes:
1: Severidad de la enfermedad;
2: Mejoría global;
3: Efectos terapéuticos;
4: Efectos adversos.
Es una escala muy usada para la investigación y prueba de nuevas drogas en la fase 3 y 4, cuando es necesario una rápida examinación objetiva del resultado clínico del fármaco en investigación (Ver el siguiente cuadro).
Cuadro 19. Impresión clínica global (Clinical Global Impression, CGI)
Enjuicie la gravedad de la enfermedad y los cambios sucedidos en el cuadro clínico. Tilde en cada caso la casilla correspondiente. Establezca a continuación el índice de efectividad de la medicación, marcando con sendos tildes el par de casillas correspondientes. En cada apartado se debe elegir tina y sólo una respuesta. Los puntos 2 y 3 pueden omitirse en la evaluación inicial, marcando «no evaluado», para ambos puntos.
Escala para la evaluación de la ansiedad de Hamilton
Consta de 14 ítemes y permite un rastreo rápido de la ansiedad psíquica y somática. Es de fácil administración y sus puntajes se evalúan como:
leve (14 puntos),
moderado (14-28 puntos),
grave (28-42 puntos),
42-66 (incapacidad total).
Cuadro 20. Escala de Hamilton (ansiedad)
0: Ausente; 1: Leve; 2: Moderado; 3: Grave; 4: Totalmente incapacitado
1) Estado ansioso:
Preocupaciones, temor de que suceda lo peor, temor anticipado, irritabilidad.
2) Tensión:
Sensación de tensión, fatigabilidad, sobresalto al responder, llanto fácil, temblor, sensación de inquietud, imposibilidad de relajarse.
3) Temores:
De la oscuridad, de extraños, de ser dejado solo, de animales, del tráfico, de las multitudes.
4) Insomnio:
Dificultad para conciliar el sueño. Sueño interrumpido. sueño insatisfactorio y sensación de fatiga al despertar, sueños, pesadillas, terrores nocturnos.
5) Intelectual:
Dificultad de concentración. memoria pobre.
6) Estado depresivo:
Pérdida del interés. Falta de placer en los pasatiempos, depresión, despertar temprano, trasposición de sueño y vigilia.
7) Sistema somático:
Dolores y mialgias, espasmos musculares o calambres, rigidez, tics mioclónicos, rechinar de dientes, voz vacilante, tono muscular aumentado.
8) Sistema somático (sensorial):
Tinitus, visión borrosa, oleadas de frío y calor, sensación de debilidad, sensación de prurito.
9) Síntomas cardiovasculares:
Taquicardia, palpitaciones, dolor precordial, pulsaciones vasculares pronunciadas, sensación de desmayo, arritmia.
10) Opresión o constricción torácica, sensación de ahogo, suspiros, disnea.
11) Síntomas gastrointestinales:
Dificultad al deglutir, flatulencia, dolor abdominal, sensación de ardor, pesadez abdominal, náuseas, vómitos, borborismos, heces blandas, pérdida de peso, estreñimiento.
12) Síntomas génito-urinarios:
Polaquiuria, micción urgente, amenorrea, menorragia, frigidez, eyaculación precoz, pérdida de libido, impotencia.
13) Síntomas del sistema nervioso vegetativo:
Sequedad bucal, rubor, palidez, tendencia a la sudoración, vértigo, cefaleas por tensión, erectismo piloso.
14) Comportamiento durante la entrevista:
Inquietud, impaciencia o intranquilidad, temblor de manos, fruncimiento del entrecejo, rostro preocupado, suspiros o respiración rápida, palidez facial, deglución de saliva, eructos, tics.
Cuestionario de cogniciones agorofóbicas (Agarofobic cognitions questionnaire, ACQ)
Consta de 14 ítemes, puntúa síntomas de inquietud y temor en relación con la ansiedad agarofóbica. La pregunta acerca del detalle sintomático es altamente descriptiva y de una muy buena definición de rastreo signológico. Es muy fácil su uso y es indicada para la evaluación del proceso de ansiedad respecto de una psicoterapia y/o de un agente farmacológico.
La tabla de puntajes es:
rara vez (14-28),
a veces (28-42),
frecuentemente (42-56),
siempre (56).
Escala para la evaluación de la depresión de Hamilton (cuadro 21)
Esta escala posee las siguientes ventajas:
a) su buena validez y confiabilidad,
b) es de uso internacional,
c) mide la variación diurna,
d) puntúa mejor que la escala HARD el ítem del aumento o pérdida de peso.
Sin embargo existen críticas como que: la puntuación no está repartida en el mismo número de escalas nominales; el subítem 15 (hipocondría, no tiene buenas preguntas de consigna); es algo extensa; el subítem 19 (despersonalización y fuera de la realidad), es de pobre evaluación y no posee diseño y buena silueta diagnóstica para medir gravedad excepto su puntaje total.
La más conocida es la versión con 19 ítemes: leve (13.5-27 puntos); moderado (13.5-27 puntos); grave (30.5-54 puntos); incapacitado (54 puntos).
Cuadro 21. Escala de Hamilton (depresión)
1. ESTADO DEPRESIVO
0: Ausente; 1: Presente solamente si se le pregunta; 2: Expresado espontáneamente por el paciente; 3: Se manifiesta a través del comportamiento del paciente (expresión facial, postura, voz, tendencia al llanto); 4: El paciente expresa este estado en su espontánea comunicación, verbal y no verbal.
2. CULPA
0: Ausente; 1: Auto-reproche, siente que defrauda a la gente; 2: Ideas de culpa pasadas o presentes; 3: La presente enfermedad es un castigo; 4: Escucha voces acusatorias o denunciantes o experimenta alucinaciones visuales.
3. SUICIDIO
0: Ausente; 2: Cree que no vale la pena vivir; 3: Desearía estar muerto; 4: Intento de suicidio (cada intento real = 4).
4. INSOMNIO INICIAL
0: Ausente; 1: Ocasionalmente dificultad en conciliar el sueño (más de 1/2 hora.); 2: Dificultad en conciliar el sueño habitualmente.
5. INSOMNIO MEDIO
0: Ausente; 1: Paciente inquieto y molesto durante la noche; 2: Despertándose completamente durante la noche. Se levanta (no solamente para orinar).
6. INSOMNIO TARDÍO
0: Ausente; 1: Inquieto y molesto en horas tempranas pero se vuelve a dormir; 2: Despertándose completamente por la madrugada e incapaz de reanudar el sueño.
7. TRABAJO E INTERÉS
0: No hay dificultad; 1: Sentimiento de incapacidad: distracción, indecisión y vacilación en el trabajo o hobbies; 2: Pérdida de interés en el trabajo o hobbies, debe obligarse a realizarlas. Lo dice él mismo o se reconoce durante la entrevista; 3: Disminución en la productividad; incapaz de trabajar eficientemente. En internados menos de 3 horas de trabajo con propia iniciativa; dejó de trabajar debido a la enfermedad actual. En internados no desarrolla ninguna actividad.
8. RETRASO
0: Pensamiento y conversación normal; 1: Leve atraso en la entrevista; 2: Entrevista difícil; 3: Estupor completo.
9. AGITACIÓN
0: Ausente; 1: Inquietud con las manos 0 similar; 2: Retorcerse las manos, morderse los labios, etc.
10. ANSIEDAD PSíQUICA
0: Ausente; 1: Tensión e irritabilidad subjetiva; 2: No se preocupa por asuntos sin importancia; 3: Angustia aparente en facies y conversación; 4: La ansiedad se manifiesta espontáneamente.
11. ANSIEDAD SOMÁTICA
0: Ausente; 1: Leve; 2: Moderada; 3: Severa; 4: Lo incapacita.
12. SÍNTOMAS SOMÁTICOS GASTROINTESTINALES
0: Ausente; 1: Disminución del apetito, pero come sin que se lo presione; 2: Debe exigirse que coma. Exige o requiere laxantes o medicación gastrointestinal.
13. SÍNTOMAS, SOMÁTICOS GENERALES
0: Ausente; 1: Pesadez en los miembros, espalda o cabeza. Dolor de la espalda o pérdida de energía y fatigabilidad; 2: Síntomas anteriores muy intensos.
14. SÍNTOMAS GENITALES
0: Ausente; 1: Leves; 2: Severos.
15. HIPOCONDRÍA
0: Ausente; 1. Autoabsorción (corporalmente); 2: Preocupación por la salud física; 3: Actitud quejosa por su salud física. Reclama ayuda, etc.
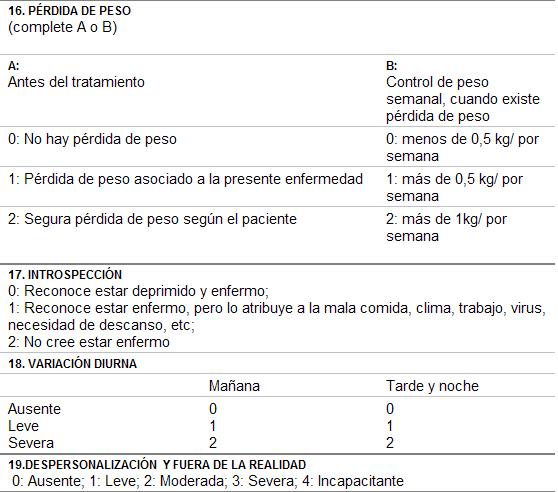
Escala para la evaluación de la depresión HARD (Diagrama de Depresión HAEP, de Rufin y Ferreri)
Consta de cuatro subescalas que son: 1: Humor; 2: Angustia; 3: Enlentecimiento y 4: Peligro.
Luego de haberla utilizado durante varios años, hemos podido constatar las siguientes ventajas, respecto de otras escalas:
1) Posee un buen diseño estructural global, que permite seguir la evolución sindrómica del paciente evaluando constantemente la mejoría/gravedad a través de un diagrama de cuatro polos: Humor-Angustia-Enlentecimiento-Peligro (HAEP).
2) La subescala de Peligro es útil para medir síntomas de depresión psicótica e ideación suicida.
3) Presenta la posibilidad de efectuar sumatorias totales de cada ítem H, A,E, P.
4) Al proponer un diseño o gráfico diagnóstico, además de objetivar el tipo de depresión, permite el seguimiento del antidepresivo por su perfil clínico (sedativos, activantes, etc.).
5) Brinda el subtest de ‘figura sumergida»: una vez que se transportan los puntajes de cada subescala a la diagonal numérica que corresponda, se unen los cuatro puntos obtenidos en el gráfico, se logra así una figura geométrica. Se traza luego una línea que cruce horizontalmente el eje del diagrama (cuadrado negro), de forma tal que esta línea divide la figura geométrica en dos. De acuerdo con el porcentaje del total de la superficie de la figura geométrica que esté por debajo de la línea trazada, corresponderá la asignación de un valor de vigilancia sobre el enfermo, dado que mide los ítemes de Peligro y Ansiedad: entre un 40 y un 50 % de «figura sumergida», requiere una vigilancia moderada del paciente, por arriba del 50 % la misma debe ser permanente debido al riesgo suicida.
Tiene las desventajas de que su uso se encuentra poco difundido en nuestro medio, el ítem referido al aumento o pérdida de peso sólo evalúa la pérdida de peso y es más compleja que evaluar que la escala de Hamilton. La puntuación es:
leve (20-34),
moderada (35-49) y
grave (50-72).
Cuadro 22: Escala de depresión H.A.E.P. (Puntajes H+A+E+P)
1) HUMOR (Puntaje total H)
Tristeza
0: Ausente; 1-2: Parece desalentado, pide que se le ayude; 3-4: Pesimismo expresado espontáneamente o al preguntarle. Tristeza aparente (por los gestos, la actitud, la voz, la tendencia a llorar); 5-6: Sentimiento profundo de desesperanza expresado verbalmente y/o con la actitud.
Desinterés
0: Interés habitual por el mundo y por los demás; 1-2: Disfruta menos con las cosas que antes le eran placenteras; 3-4: Menor interés por los demás, el mundo que lo rodea carece de interés; 5-6: Replegado sobre sí mismo, y su preocupación pesimista; inercia dolorosa de las emociones (nada me afecta).
Apetito
0: Normal; 1-2: Algo disminuido; 3-4: Encuentra la comida insípida; se esfuerza para comer; 5-6: Sólo come si se lo obliga.
2) ANGUSTIA (Puntaje total A)
Ansiedad Psíquica
0: Tranquilo; 1-2: Inquieto. Tensión inhabitual pero pasajera; 3-4 Sentimiento permanente de tensión interior. Espera dolorosa. Crisis de ansiedad intermitente; 5-6: Ansiedad mayor, duradera. Confusión (perplejidad).
Ansiedad Somática
0: Ausente; 1-2: Discreta: preocupaciones corporales frecuentes, dispepsia, algias diversas; 3-4: Mediana: trastornos vasomotores, extremidades frías, sofocos, sensación de ahogo, cefaleas, náuseas, trastornos del tránsito intestinal, palpitaciones, crisis de bulimia; 5-6: Angustia importante: estos trastornos se vuelven permanentes e incapacitantes.
Insomnio
0: Sueño normal; 1-2: Insomnio al inicio de la noche; 34: Despertar frecuente. Sueño reducido (Interrumpido al menos durante 2 horas), agitado, con pesadillas, poco reparador; 5-6: Menos de 3 horas de sueño en 24 horas. Insomnio habitual de madrugada (sin poder volver a dormirse).
3) ENLENTECIMIENTO (Puntaje total E)
Cansancio
0: Ausente; 1-2: Dificultad para iniciar actividades (profesionales, escolares, domésticas). Predominio matutino de la astenia; 3-4: Sentimiento penoso de necesitar un esfuerzo para la realización de las actividades cotidianas. Sensación intermitente de estar «vacío», «bloqueado»; 5-6: Cansancio extremo. Agotamiento permanente, Incapacidad de actuar sin ayuda.
Concentración
0: Sin dificultad; 1-2: Necesidad de un esfuerzo; 34: Sentimiento de disminución de las capacidades intelectuales (atención, concentración, memoria), comprobado con la lectura, la conversación, el cálculo, la televisión; 5-6: Trastornos que dificultan la consulta. Dificultad de comprensión y de memorización para cosas habituales.
Actitud
0: No hay aparentemente enlentecimiento; 1-2: Gestos, lenguaje o movimientos algo más lentos; 34: Gestos, lenguaje o movimientos claramente lentos; 5-6: Enlentecimiento que dificulta la consulta.
4) PELIGRO (Puntaje total P)
Desvalorización
0: Ninguna; 1-2: Sentimiento de inferioridad; pérdida de la autoestima si se le pregunta directamente; 3-4: Expresión espontánea de sentimientos inquietantes de desvalorización «no valgo nada, soy un ser inferior»; 5-6: Ideas delirantes de autodesprecio «soy una basura»,
Ideas de suicidio
0: Ninguna; 1-2: Se hace preguntas sobre la necesidad de vivir; 34: «Malas ideas negras». El suicidio se considera una solución si el tratamiento no aporta una mejoría; 5-6: Intenciones suicidas manifiestas. Intento de suicidio reciente.
Ideas delirantes (de culpabilidad, y/o de ser incurable, y/o de persecución)
0: Ninguna; 1-2: Deformación de la realidad: lo ve todo negro»; 3-4: Visión alterada del mundo, dominada por las sospechas, el drama, la ausencia de soluciones; 5-6: Autoacusación clara. Ideas delirantes de indignidad, de incurabilidad, de hipocondría, de ruina, de persecución. Alucinaciones amenazadoras.
Escala para la evaluación de la depresión de Montgomery y Asberg (Montgomery Asberg Depression Rating Scale)
Más conocida y desarrollada en los países europeos. Se diferencia de la de Hamilton por ser más corta (tiene 10 ítemes), las consignas son rápidas y claras y permite diferenciar con mayor rapidez las depresiones leves de las graves. Clasifica el ánimo de tristeza en 2 ítemes y en otros 2 los pensamientos pesimistas y suicidas, lo que significa que el 40 % de la entrevista es para estos 4 ítemes. De esta forma es fácil incorporar o desechar los pacientes graves, a un nuevo estudio con antidepresivos. Toda la escala puede clasificarse con categorías definidas (24-6) o intermedias (P3-5).
Cuadro 25. Escala de depresión Montgomery-Ásberg (Mädrs)
La evaluación se basa en una entrevista clínica partiendo de preguntas formuladas de manera vaga acerca de los síntomas, hasta llegar a preguntar más detalladas que permitan una precisa evaluación de la gravedad. El entrevistador debe decidir si la evaluación se amolda a los niveles definidos en la escala (0-2-4-6) o a los niveles intermedios (1-3-5).
Debe señalarse que sólo raras veces un paciente deprimido no puede evaluarse con los ítemes de esta escala.
En caso de que no puedan obtenerse respuestas adecuadas y definidas de] paciente, deben utilizarse todos los datos relevantes así como otras fuentes de información, de acuerdo con la práctica clínica habitual.
1) TRISTEZA MANIFIESTA
Se refiere a abatimiento, desánimo, desesperación, que se refleja en el habla, en la expresión facial y en la actitud.
0: No hay tristeza,
1-2: Parece desanimado, pero se anima o alegra con dificultad,
3-4: Parece triste y poco feliz la mayor parte del tiempo,
5-6: Parece muy triste y desdichado todo el tiempo, extremadamente abatido.
2) TRISTEZA EXPRESADA
Se refiere a las quejas del paciente respecto de su estado de ánimo deprimido. Independientemente de que éste se refleje en su apariencia o no. Incluye estar bajo de ánimo, desmoralizado, desesperanzado, con la creencia de que no se lo puede ayudar. Evaluar de acuerdo con la intensidad y duración, teniendo en cuenta hasta qué punto el humor depresivo esta influido por acontecimientos externos.
0: Tristeza ocasional, de acuerdo con las circunstancias,
1-2: Triste o bajo de ánimo, pero se alegra o anima con dificultad,
3-4: Sentimiento generalizado de tristeza o abatimiento. El ánimo está influenciado por las circunstancias externas,
5-6: Tristeza, desmoralización o abatimiento continuos e invariables.
3) TENSIÓN INTERNA
Se refiere a sentimientos de malestar poco definidos, irritación, agitación interna, tensión mental llegando al pánico, terror o angustia extrema. Evaluar de acuerdo con la intensidad, frecuencia, duración y la ayuda requerida.
0: Sereno y tranquilo, tensión interior pasajera,
1-2: Sentimientos ocasionales de malestar mal definido e irritabilidad,
3-4: Sentimientos continuos de tensión interna o pánico intermitente, sólo con dificultad el paciente puede controlar;
5-6: Terror o angustia extrema. Pánico insoportable.
4) INSOMNIO
Se refiere a la experiencia subjetiva de disminución en la duración o profundidad del sueño, comparado con el patrón normal del paciente.
0: Duerme poco;
1-2: Ligera dificultad para conciliar el sueño o ligera reducción, sueño superficial o entrecortado;
3-4: Sueño reducido o entrecortado por lo menos durante dos horas;
5-6: Duerme menos de 2-3 horas.
5) DISMINUCIÓN DEL APETITO
Se refiere al sentimiento de pérdida de apetito en comparación con su patrón habitual estando bien. Puntuar de acuerdo con la pérdida del deseo de comer o la necesidad de autoforzarse para comer.
0: Apetito normal o aumentado;
1-2: Apetito ligeramente disminuido;
3-4: Sin apetito. Los alimentos no le saben a nada;
5-6: Necesita ser persuadido.
6) DIFICULTADES DE CONCENTRACIÓN
Se refiere a dificultades para concentrarse en sus pensamientos, llegando a una total incapacidad para ello. Puntuar de acuerdo con la intensidad, frecuencia y el grado de incapacidad.
0: No hay dificultades para concentrarse;
1-2: Dificultades ocasionales para concentrarse en sus pensamientos;
3-4: Dificultades para concentrarse y mantener esa concentración;
5-6: Incapacidad para leer o conversar sin grandes dificultades.
7) INHIBICIÓN PSICOMOTRIZ
Se refiere a dificultades para «arrancar» o a la lentitud para iniciar las actividades cotidianas.
0: Casi ninguna dificultad para «arrancar». No hay pereza;
1-2: Dificultades para iniciar las actividades;
3-4: Dificultades para iniciar actividades rutinarias simples, que se prosiguen con
esfuerzo;
5-6: Lasitud completa. Incapacidad de hacer lo que sea sin ayuda.
8) INCAPACIDAD DE SENTIR AFECTOS
Se refiere a la experiencia subjetiva de disminución del interés por el entorno o por actividades placenteras.
0: Interés normal por su entorno y otras personas;
1-2: Interés reducido para disfrutar de las actividades habituales;
3-4: Pérdida de interés por el entorno, pérdida de sentimientos hacia parientes y amigos íntimos;
5-6: Experiencia de estar paralizado emocionalmente. Incapacidad de sentir rabia, pena o placer y una completa e incluso dolorosa incapacidad para tener sentimientos hacia parientes y amigos íntimos.
9) PENSAMIENTOS PESIMISTAS
Se refiere a pensamientos de culpa, inferioridad, autorreproche, pecado, remordimiento y desolación.
0: No hay pensamientos pesimistas;
1-2: Ideas fluctuantes de fracaso, autorreproche y autodepreciación;
3-4: Autoacusaciones persistentes, claras pero todavía ideas racionales de culpa o pecado. Pesimismo creciente en relación con el futuro;
5-6: Ideas obsesivas de empobrecimiento, remordimiento o pecado imperdonable. Autoacusaciones absurdas e inquebrantables.
10) PENSAMIENTOS SUICIDAS
Se refiere al sentimiento de que no vale la pena vivir, de que una muerte natural sería bienvenida. Pensamientos o preparativos de suicidio. Los intentos de suicidio no 11 per se» influencian los puntajes.
0: Disfruta de la vida o la toma como viene;
1-2: Cansado de la vida. Pensamientos pasajeros de suicidio;
3-4: Se sentiría mejor muerto. Considera al suicidio como tina posible solución pero no hay todavía planes o intenciones precisas;
5-6: Planes precisos de suicidio en cuanto se le presente una oportunidad. Preparativos para suicidarse.
Escala de evaluación psiquiátrica breve
(Brief Psychiatric Rating Scale, BPRS)
La mayoría de las investigaciones de origen norteamericano con psicofármacos antipsicóticos la incluyen. Sus beneficios incluyen una entrevista en tres fases y dieciocho ítemes de evaluación de síntomas, los cuales dan lugar a cinco factores de medición.
La escasez de detalles en la guía de la entrevista y la ausencia de definición para los siete puntos anclados a lo largo de la escala hace que se diferencie según el entrevistador. No fue diseñada para puntuar los síntomas negativos de la esquizofrenia (sólo incluye tres ítemes negativos: afectos embotados, retiro de la emoción y retardo motor). Se ha encontrado que esos síntomas son valiosos para la correlación con estados depresivos y catatónicos y para las confusiones con síntomas extrapiramidales. Estos tres síntomas negativos responden diferencialmente a los neurolépticos, lo que sugiere que conceptualmente pueden ser distinguidos pero no combinados.
La BPRS negativa o la subescala de la retirada del retardo, como fue llamada, considera solamente dos esferas funcionales: la emocional y la motora. El factor anergia de la BPRS, que algunos investigadores han utilizado como escala negativa, incluye los ítemes mencionados más la desorientación, los cuales son síntomas multideterminantes que podrían ser asociados con confusión, abstinencia (retiro de drogas) o neuropatologías.
Escala para la evaluación de los síntomas negativos de la esquizofrenia
(Scale for the Assessment of Negalive Symptoms, SANS) y Escala para la evaluación de los síntomas positivos de la esquizofrenia (Scale for the Assessment of Positive Symptoms, SAPS)
La SANS apareció como la primer escala para evaluar de manera específica los fenómenos negativos en la esquizofrenia, con gran ascendencia en los EE.UU. La principal ventaja fue la detallada y confiable inspección de cinco síntomas negativos: alogia (falta de espontaneidad y fluidez en el pensamiento y la conversación), anhedonia (pérdida del placer y escaso contacto social), embotamiento afectivo (falta de fluidez para expresar emociones), pérdida volitiva (pérdida de la habilidad para empezar y terminar las tareas; apatía; anergia) y déficit atencional.
Cuando es usada acompañada con los cuatro ítemes de la de la escala para la evaluación de los síntomas positivos (SPAS): alucinaciones, delirios severos, alteración marcada del pensamiento abstracto y conductas bizarras y desorganizadas, resulta algo extensa por el disbalance entre el número de ítemes de la SANS y de la SAPS.
Una severa crítica que se les realiza a este tipo de escalas globales es que determinan lo que se llama «un score o resultado final», siendo pobres en la calidad objetiva y descriptiva. En suma, la construcción de la escala que incluye seis puntos resulta escasa para un adecuado anclaje de las definiciones Y un autointerrogatorio bien estructurado o formalizado. En consecuencia muchas investigaciones han reportado gran disconformidad con la SANS, teniendo dificultades en establecer una buena confiabilidad y validez. Por ejemplo, no fue utilizada comparativamente en estudios con pacientes depresivos.
La escala para la evaluación de los síndromes positivo y negativo
(Positive and Negative Syndrome Scale for Schizophrenia, PANSS) (cuadro 26)
La PANSS fue desarrollada y estandarizada para la evaluación tipológica y dimensional de¡ fenómeno esquizofrénico. Inicialmente fue formulada como una adaptación especial de la BPRS y de la Psychopatology Rating Schedule (PRS).
Este instrumento de evaluación de treinta ítemes (en 7 categorías desde ausencia hasta presencia extrema) consta de tres subescalas: positiva, negativa y de psicopatología general. Se basa en una entrevista clínica formal, de características semiestructurada.
De los treinta ítemes, siete están agrupados para formar la escala positiva. Otros siete constituyen la escala negativa, que mide los rasgos ausentes, de lo que sería un estado mental normal. Basado en la diferencia entre ambas subescalas se encuentra la de psicopatología general bipolar, de 16 ítemes, que especifica el grado de predominio de un síndrome sobre otro.
Su uso está validado, es de rápida administración y reúne en sí misma todos los elementos necesarios para la obtención de una adecuada información del tipo y nivel de síntomas esquizofrénicos del sujeto entrevistado.
Diferencia las esquizofrenias I y II y permite una adecuada implementación del abordaje psicofarmacológico. Es, por ejemplo, posible definir la esquizofrenia de tipo II, y utilizar los neurolépticos atípicos desde el comienzo.
Es de utilidad para una interpretación adecuada con otros estudios complementarios realizados por métodos neuroquímicos y de imágenes (SPECT), que demuestren alteraciones manifiestas según se trate de esquizofrenia I o II. (8, 18, 23, 46, 73).
En una encuesta oral, que realizamos a un grupo de 140 profesionales acerca del uso de escalas objetivas para realizar el diagnóstico del tipo de esquizofrenia, sólo 8 profesionales (6 %) utilizaban algún tipo de escala y cinco de ellos (4 %) realizan el diagnóstico del tipo III de esquizofrenia. El resto lo hacía según la impresión clínica o subjetiva. (Encuesta sobre uso de escalas en esquizofrenia, 1995).
Si bien no se conoce una investigación sistemática respecto de la frecuencia de utilización del tipo III, observamos que el diagnóstico del mismo prácticamente no se realiza, ya que no aparece en las historias clínicas.
Escala de calidad de Vida
La escala de calidad de vida consta de 10 ítemes, los cuales condensan tres factores que se reflejan en tres áreas funcionales (salud, conducta laboral, interacción social). Por contraste con otras escalas, pone más énfasis en lo social, lo ocupacional y en los datos comportamentales más que en el juicio psicopatológico.
Cuadro 27. Escala de calidad de vida
1. En general, Ud. podría decir que su salud es:
Excelente (1), Muy Buena (2), Buena (3), Regular (4), Pobre (5)
2. Por favor elija la respuesta que mejor describe cuán verdadero o falso es cada uno de los siguientes ítemes para Ud:.
Definitivamente verdadero (1), Casi siempre verdadero (2), No estoy seguro (3), Casi siempre falso (4), Definitivamente falso (5):
a) Comienzo a sentirme enfermo un poco antes que otras personas. b) Soy más saludable que cualquier persona que conozco.
c) Estoy a la expectativa de que empeore mi salud.
d) Mi salud es excelente.
3. Durante las últimas dos semanas, ¿cuántos días se quedó en cama por su salud más de medio día?
Número de días:
4. Cómo se sintió las últimas dos semanas:
Todo el tiempo (1), La mayor parte del tiempo (2), Buena parte del tiempo (3), Algo del tiempo (4), Una pequeña parte del tiempo (5),
a) ¿Se sintió rendido o agotado?
b) ¿Tuvo un montón de energía?
c) ¿Se sintió lleno de energía?
d) ¿Tuvo suficiente energía para hacer las cosas que quiso?
e) ¿Se sintió cansado?
5. Para cada una de las siguientes preguntas, Por favor marque con un círculo el número de la respuesta que se acerca a la forma que se sintió durante las últimas dos semanas.
Todo el tiempo (1) . La mayor parte del tiempo (2). Una gran parte del tiempo (3). Algunas veces (4). Pocas veces (5). Nunca (6):
a) ¿Cuánto tiempo tuvo dificultad en razonar, resolver problemas, como por ejemplo: hacer programas, tomar decisiones, aprender cosas nuevas?
b) ¿Cuánto tiempo se olvidó por ejemplo de cosas que pasaron recientemente, dónde puso cosas, compromisos?
c) ¿Cuánto tiempo tuvo problemas en mantener su atención en cualquier actividad por un tiempo prolongado?
d) ¿Cuánto tiempo tuvo dificultad en hacer actividades que involucren concentración y pensamiento?
6. Estos ítemes describen la conducta de alerta y el pensamiento. Por favor marque sólo aquellos Ítemes que lo describen a Ud. hoy y que están relacionados con su estado de salud.
a) Estoy confundido y comienzo a hacer más de una cosa a la vez.
b) Tengo más accidentes menores, por ejemplo, me tropiezo y me caigo, tiro cosas, me choco con las cosas.
c) Respondo lentamente a cosas que están hechas o dichas. d) No termino las cosas que empiezo.
e) Tengo dificultades razonando y solucionando problemas, por ejemplo, haciendo planes, tomando decisiones, aprendiendo cosas nuevas.
f) A veces me siento confundido, por ejemplo, no sé dónde estoy, quién está a mi alrededor, o qué día es.
g) Olvido mucho, por ejemplo, hechos que pasaron recientemente, dónde puse cosas, o asistir a citas.
h) No pongo atención en ninguna actividad. i) Cometo más errores de lo usual.
j) Tengo dificultades haciendo cosas que involucren pensamiento y concentración.
Conducta laboral
El próximo grupo de ítemes tiene que ver con cualquier trabajo que Ud. haya realizado en las últimas dos semanas (pregunta 7), incluyendo cualquier tarea del hogar (pregunta 8). Trabajo significa cualquier cosa que Ud. considere que hace regularmente.
Estoy trabajando actualmente:
Si es «Sí», responda las preguntas 7 y 8
Si es «NO», sólo responda la pregunta 8.
7. «SI»
Durante las últimas dos semanas: Totalmente de acuerdo (1), Muy de acuerdo (2), Generalmente de acuerdo (3), Generalmente en desacuerdo (4), Muy en desacuerdo (5), Totalmente en desacuerdo (6).
a) Me sentí entusiasmado acerca de mi trabajo.
b) No hice m¡ trabajo cuidadosamente ni con la precisión habitual.
c) Me sentí cansado o somnoliento en el trabajo.
d) No me sentí talentoso o hábil en el trabajo como siempre. e) No he tenido problemas en concentrarme en el trabajo.
f) He estado capacitado para mantenerme a la altura de mi trabajo.
8. «NO»
Durante las últimas dos semanas
a) He trabajado en derredor de la casa sólo por períodos cortos de tiempo y he tenido que descansar a menudo.
b) He tenido dificultad en hacer tareas que involucren pensamiento y concentración.
c) No logro realizar las tareas hogareñas.
d) Yo estaba capacitado para mantenerme a la altura (lidiar) con las tareas hogareñas.
e) No me molesta hacer las tareas hogareñas.
9. Interacción social
Los siguientes ítemes describen cómo Ud. ha actuado las últimas dos semanas. Por favor lea cada ítem, y luego marque con un círculo uno de los números en cada línea para indicar el grado de acuerdo con la descripción del ítem. Algunos ítems pueden parecer iguales a otros, pero cada uno es diferente y puede ser calificado por sí solo:
a) He mostrado menos interés en los problemas de otras personas, por ejemplo, no he escuchado cuando me contaban sus problemas, no ofrecí ayuda.
b) Actué de manera irritable hacia los que me rodean, por ejemplo, respondí de manera violenta, me burlé de la gente, critiqué frecuentemente a los demás.
c) He demostrado menos afecto.
d) He reclamado constantemente, por ejemplo, insistiendo a otros en hacer cosas por mí, diciéndoles cómo hacer las cosas.
e) He actuado de manera desagradable con miembros de mi familia, por ejemplo, actué con maldad, he sido obstinado.
f) He puesto menos atención en mi familia y/o amigos.
g) No he actuado como solía hacer cuidando a mi familia y/o amigos.
h) No me he divertido con mi familia y/o amigos como solía divertirme.
10. Qué tan satisfecho está Ud. con su vida en su totalidad
(marque un n°)
Completamente satisfecho (1), Muy satisfecho (2), Satisfecho (3), Neutro
(4), Insatisfecho (5), Muy insatisfecho (6), Completamente insatisfecho (7).
1-25. Psiconeurobiología clínica de los trastornos de ansiedad
La Región de Trauma Cerebral formada por la amígdala, el locus coeruleus y el eje HPA, activada de forma crónica por el estrés, procesa las señales de manera tan veloz, que sus acciones se independizan del control que ejercía la corteza frontal.
Recientemente se han descubierto centros y circuitos especializados en la psiconeurobiología de la ansiedad que han cambiado el concepto de procesamiento. Este término integra mecanismos de la percepción, en diferentes centros neuroanatómicos, que forman circuitos, que relacionados, a través de una red interneuronal, pueden organizar respuestas en relación con el medio. La evolución de la especie, además de producir la especialización en diferentes centros (por ejemplo, la corteza rinal y el bulbo olfatorio evolucionaron, en un sentido anatómico, dando lugar a la aparición de la corteza frontal inteligente), logró que el funcionamiento del cerebro esté determinado por diferentes sub-sistemas integrados con un alto grado de diferenciación y autonomía. Estos conceptos de autonomía e independencia funcional de las diferentes unidades o circuitos cerebrales revolucionaron el modo de comprender el comportamiento humano.
Los trastornos de la ansiedad, las reacciones de alarma, la formación de la emoción producida por un estímulo medio ambiental y el trastorno por estrés postraumático (Postraumatic Stress Disorder, PTSD), pueden ser en la actualidad estudiados de acuerdo a las nuevas formulaciones de estos sistemas.
La amígdala (del griego almendra), es un centro de alta especialización en lo que respecta al procesamiento de las emociones y las reacciones de alarma. Por ejemplo la formación de las lágrimas depende de la interconexión de la amígdala con el cíngulo. Las mismas se producen por un estímulo emocional ocasionado por el medio ambiente, en un recuerdo almacenado en una proteína, que depende de un microcircuito de alta especialización (emoción-reacción-respuesta), en este microsistema de la amígdala con el cíngulo. Si se extirpa o se destruye este microsistema no habría posibilidad de la producción de lágrimas.
El sistema gabaérgico está relacionado directamente con la ansiedad. Se encuentran neuronas gabaérgicas en el bulbo olfatorio, el cerebelo, la corteza piriforme, el tubérculo cuadrigémino superior, el globus pallidus, el hipocampo, el hipotálamo, la protuberancia, el locus niger y los cuerpos estriados.
Las acciones gabaérgicas sobre este sistema, a nivel farmacológico son desarrolladas en los capítulos 4 y 8, aquí se hará referencia al concepto del sistema o unidades conocido como «Región del Trauma Cerebral» (Brain Trauma Center, BTC).
En los trastornos de ansiedad interactúan diferentes estructuras como son el cerebro límbico, el hipotálamo anterior y posterior, el locus coeruleus, la formación reticular, la corteza piriforme y las glándulas suprarrenales. La hormona liberadora de corticotrofina (CRH), va a producir sus acciones farmacológicas en todas estas zonas, conocidas como BTC. (ver cap, 2, 2-2)
El CRH, está compuesto por 41 aminoácidos, se forma en las neurona peptidérgicas del núcleo paraventricularis del hipotálamo y es el factor específico de activación de la ansiedad (ver cap. 2).
La hipótesis clásica, aun hoy vigente, relaciona a la ansiedad con la arginina, la vasopresina, la ocitocina, la adenosina, el cortisol y el CRH. Sin embargo, en la actualidad, hay que integrar a la misma los efectos metabólicos que produce el CRH sobre todas estas formaciones cerebrales.
Se pudo comprobar, que el estrés o los factores de desestabilización iniciales, en los trastornos por ansiedad y por estrés postraumático, es el complejo formado por el CRH-interleuquina y por el CRH-cortisol, respectivamente. Estos trastornos se desencadenan, cuando el CRH -sintetizado en el núcleo paraventricularis-, activa farmacológicamente la ACTH y la «región del trauma cerebral» (BTC). En el primer caso, el CRF actúa sobre la adenilciclasa, que genera reacciones sobre la arginina, la vasopresina, la ocitocina y los glucocorticoides; y en el segundo, por la estimulación patológica persistente sobre el BTC.
El centro de trauma cerebral está integrado por tres zonas:
1) el eje hipotálamo-hipofiso-suprarrenal,
2) la amígdala, y
3) el locus coeruleus.
Esta zona actúa, desde el punto de vista práctico, como un sistema cerrado que, recibe, reconoce, resuelve, procesa y almacena, en forma casi autónoma, los estímulos de carácter emocional. Tiene múltiples vías de conexión, pero las más importantes son a través del cíngulo y del septo, con el área cortico-subcortical y, por medio de la amígdala, con el locus coeruleus, la estria terminalis, etc.
Luego de reconocer el estímulo estresógeno, por medio de una verdadera «network» o red intersistémica se activarán sistemas defensivos de adaptación. La CRH y los glucorticoides originados tratan de «adaptarse» a la nueva situación, produciendo fenómenos inhibitorios (reducción del los linfocitos, de la reacción antígeno-anticuerpo) . Pero cuando el sistema de afrontamiento o «coping», no es el adecuado se generará una retroalimentación o «feedback positivo o desinhibitorio», que dará origen a un sistema de señales ajeno a la conciencia (corteza-subcorteza cerebral) con aumento de la descarga noradrenérgica, que producirán diversos trastornos (pánico, ansiedad generalizada, etc), como respuesta al estrés.
La importancia del descubrimiento de esta región BTC, se debe a su capacidad en resolver y procesar los estímulos emocionales a una elevadísima velocidad intraxónica, casi con la absoluta prescindencia de las áreas corticales. La velocidad de interconexión de la red neuronal dentro de este triángulo BTC, es muy superior a la que posee esta región con las áreas frontales. Éste sería el modelo de las respuestas conductuales impulsivas y explosivas, que se pueden organizar y pasar a la acción, sin que medie un proceso de restricción o represión formal, a cargo de las áreas más conscientes o frontales.
De esta forma la acción de este centro de trauma cerebral, podría interpretarse como parcialmente autónoma. Es decir, que cuando llega al BTC la información desde los centros superiores (áreas frontales), para efectuar una orden represiva, la respuesta formalizada por el BTC, ya se expidió.
Los tratamientos psicofarmacológicos y psicoterapéuticos actuales (por ejemplo, la psicoterapia cognitiva), estarían dirigidos a permitir respuestas, con censura racional previa, tratando de lograr el «desaceleramiento» de la velocidad intraxónica de este área.
Muchos pacientes con caracteres violentos, impulsivos o explosivos relatan que frente a un estímulo llegan a reaccionar en forma automática, no pudiendo impedir, aunque lo piensen, su acción motriz.
Las funciones de la «Región del Trauma Cerebral» se caracterizan por tener autonomía, automatismo y capacidad de almacenar la memoria emocional.
El CRH está directamente asociado con la conservación de la vida y sus acciones estimulantes son necesarias para la subsistencia. Por lo tanto, no se podría afirmar que su acción es negativa sino que la estimulación del CRH sobre la BTC es la patológica.
En el individuo normal, frente a un estímulo, el CRH recorre un camino que empieza en el núcleo supraventricularis y continúa en el hipotálamo anterior, posterior, amígdala y locus coeruleus, siendo este proceso reversible, ya que presenta un «feedback» inhibitorio propio. En cambio en los pacientes con trastornos de ansiedad (generalizada y crónica) el CRH se trasloca y provoca una estimulación permanente o semipermanente sobre la amígdala y locus coeruleus, generando una neurovulnerabilidad celular con su consecuencia a nivel psiconeurobiológico.
Esta traslocación, que significa que el CRH no se puede autoinhibir y se queda «estimulando equivocadamente» la amígdala y el locus coeruleus, genera diferentes estados patológicos:
1 ) Estado de alarma automática (Self alarm).
2) Activación espontánea de tipo «kindling», con características de propagación y vulnerabilidad [acciones sobre hormonas de crecimiento (GH), tirotrófica (TSH), corticotrofina (ACTH), etc.]
3) Fenómeno de aturdimiento (High noice state). Estado fácilmente reconocible por los sujetos ansiosos, en el que se percibe un sensación de pre-desborde, definido como un «ruido interno», que no permite la ejecución de respuestas adecuadas con el medio ambiente.
Si bien los procesos neurobiológicos en la ansiedad crónica y en el trastorno por estrés postraumático (PTSD) son similares, hay diferencias en los factores de desestabilización, tanto anatómica como químicamente:
a) en la ansiedad crónica, la zona desde la cual se produce la descarga que inicia la cascada es el núcleo paraventricularis del hipotálamo y el neurotransmisor es la CRH;
b) en el PTSD la descarga inicial se produce en el hipocampo y los neurotransmisión involucrada es el sistema glutamatérgico, en acción combinada con el calcio.
En el estrés agudo, pero transitorio, los estudios realizados sobre la aplysia marina y luego comprobado en humanos, demuestran que se produce una neuromodulación de los neurotransmisores (regulación ascendente o descendente, «up o down regulation») sobre la afinidad (Kd) y sobre la densidad de sitios de recepción (Bmax). La recomendación terapéutica aquí, sería el uso de fármacos a corto plazo (por ejemplo benzodiacepinas que no sobrepasen las ocho semanas de tratamiento).
En el estrés crónico y en el PTSD los cambios son estructurales y están directamente asociados a la alteración de la expresión genética del núcleo. Es por ello que el tiempo de medicación del PTSD debe ser prolongado, ya que la acción del fármaco actuará, siempre e indefectiblemente en largos plazos, ya que lo que se intenta es la corrección de la disfuncionalidad de la alteración genética producida.
La tomografía por emisión de fotón único (SPECT) revela un aumento del flujo cerebral frontal, en la estimulación estresante aguda transitoria. En cambio, en el estrés crónico o en el paciente con PTSD, se observa un hipoflujo frontal, en general, bilateral.
La depresión que frecuentemente se asocia al PTSD, se debe entre otros factores a la disregulación metabólica del sistema noradrenérgico y dopaminérgico. Estos sujetos, desde un punto de vista psicobiológico, se comportan en forma similar a los adictos a la cocaína: aprenden a funcionar con una alta descarga de noradrenalina y dopamina. En los veteranos de guerra que presentaron PTSD, asociado a depresión, pudo observarse que el puntaje de la escala de Hamilton se encuentra disminuido, cuando éstos regresan a la cercanía de un campo de combate. Se infiere al respecto, que la descarga de glutamato-calcio vuelve a ser hiperfunción ante, devolviéndole al sujeto su nivel de hiperactivación, producto del estrés de combate.
1-26. Psiconeurobiología Clínica de las conductas violento-impulsivas y su relación con el colesterol
El colesterol interviene en los procesos de fluidez de membrana y tiene receptores intracitoplasmáticos rápidos. Su descenso en individuos hipercolesterolémicos puede desencadenar episodios de impulsividad.
Aspectos clínicos del colesterol
En la actualidad, existe un consenso científico respecto de los beneficios de la reducción del colesterol, para disminuir el riesgo de enfermedad cardiovascular. Se insiste fundamentalmente en la disminución de las lipoproteínas de baja densidad (LDL). La recomendación de la Asociación Médica Americana es la de lograr un colesterol total por debajo de 180 mg/ dl, una fracción LDL por debajo de 100 mg/dl y una fracción lipoproteica de alta densidad (HDL) por encima de 40 mg/dl, mientras que la ecuación de riesgo debe estar por debajo de 4.5.
Los beneficios reportados por la reducción del colesterol se traducen, epidemiológica y estadísticamente, en una disminución de la mortalidad por factores cardiovasculares. Sin embargo, se ha encontrado, que si bien la reducción del colesterol disminuye la muerte por factores vasculares, no ocurre lo mismo con el porcentaje de muertes totales: disminuye el riesgo de mortalidad vascular pero aumentarán otros factores de mortalidad. Cuando se investigó cuáles serían los factores de mortalidad que aumentarían en los pacientes con reducción del colesterol, se encontró que en este grupo se producía un aumento de las muertes por cáncer, accidentes violentos, suicidios y en la tasa de agresividad.
El estudio de Golier que toma una población de 700.000 sujetos con un seguimiento de 12 años, reveló en la población con bajos niveles de colesterol, un aumento de la impulsividad suicida.
Otros investigadores llegan a las siguientes conclusiones:
1) La media del grupo sin riesgo de suicidio es de 4.78-6.21 n/mol/mI, mientras que la del grupo con alto riesgo es menor a 4.5 n/mol/l.
2) A mayor velocidad de descenso del colesterol, mayor riesgo suicida.
3) Se propone que, como factor de bioseguridad, la velocidad de descenso no debería ser superior a 0.13 n/mol/1 por año, a diferencia de otros estudios, que proponen rapidez en los descensos para disminuir la mortalidad vascular.
4) En poblaciones psiquiátricas el grupo con colesterol alto o normal (7.55 n/mol/1) tenía una menor tasa de reinternaciones que el grupo con colesterol bajo (4.55 n/mol/1). (Engelberg, 1992)
Así, el descenso del colesterol se lo relaciona con el empeoramiento del ánimo, con el aumento de la violencia, con el suicidio consumado, con las muertes violentas (accidentes o crímenes) y con el aumento de los accidentes cerebrovasculares de tipo hemorrágico.
Recientemente se describió la presencia de un tono celular dependiente de los niveles de colesterol. Este tono estaría relacionado con la capacidad de respuesta celular. Sería lícito compararlo con el tono muscular, (que se define como un estado de semicontracción permanente del músculo). El tono celular marcaría la respuesta instantánea de la acción neuronal. Este «tono» estaría controlado por la corteza frontal media estriatal («medial estriatal frontal cortex, MEF), por las neuronas Ca piramidales, la serotonina y el colesterol.
El grupo de sujetos introvertidos no violentos presenta tono celular bajo, colesterol y pool serotoninérgico normal o aumentado con inhibición del sistema MEF. En cambio, el grupo extrovertido con hipertono neural, de características violentas, presenta disminución del colesterol y del pool de serotonina. Este último grupo es conocido en EE.UU. como «easy going». Estos sujetos responden a un psicotipo de sujetos irritables, se enojan, pasan al acto rápidamente y son consumidores de sustancias adictivas, fundamentalmente de bebidas alcohólicas.
El consumo de alcohol produce hipoglucemia y descenso del colesterol. Al estimular la insulina disminuye la transformación del LDL en el hígado, por acción de la inhibición de una lipasa proteica. Se estimulan de esta forma, y por vía indirecta las conductas agresivas. También se halló bajos niveles de colesterol en sujetos encarcelados, en familiares de los mismos y en personalidades de tipo asocial (70).
Se asocia la disminución del colesterol con otras causas de mortalidad, como son diferentes tipos de neoplasias. En especial se hace referencia al cáncer de hígado, de páncreas, de la zona orofaríngea y del pulmón.
Se ha dejado de lado el concepto de que el paciente oncológico debía comer para mantenerse en lo posible con sobrepeso. Como la expectativa de vida es mucho mayor, y algunas de las drogas usadas pueden aumentar el peso corporal se lo tiende a mantener en dicta. Sin embargo este tipo de pacientes deben recibir supervisión psicobiológica ya que también se ha demostrado que pueden presentar un aumento de la ideación suicida y de la depresión. Tanto la depresión como el suicidio fueron señalados como factores ligados al descenso de colesterol; por tal motivo resulta conveniente decidir la alimentación de estos pacientes en forma conjunta con el oncólogo y el nutricionista, ya que la restricción dietaria de la formación de colesterol podría aumentar su riesgo psiquiátrico.
Aspectos neurofarmacológicos del colesterol
Es interesante considerar las hipótesis de cómo el colesterol podría afectar el comportamiento, aumentando el riesgo suicida y la depresión.
Para que la neurotransmisión psicofarmacológica tenga eficacia, el psicofármaco se debe acoplar sobre la superficie de la membrana celular, para pasar al interior de la célula. Ello depende, entre otras cosas de los lípidos y proteínas de membrana y fundamentalmente de la fluidez de membrana (FM):
1 ) La fluidez de membrana tolera una variación microlipídica de hasta un 10%.
2) Entre otros elementos la fluidez depende del ácido linoleico, colesterol total, LDL, VLDL, IDL y la acción de la coenzima HMG.
3) La disminución del colesterol puede variar hasta en un 30 o 40 % la fluidez de membrana.
4) Si la fluidez de membrana, varía más de un 10 %, puede transformarse funcionalmente en pavimentosa (no es permeable).
Por lo tanto del colesterol depende, en gran parte, la fluidez de membrana y esta ultima está condicionada por la viscosidad, el transporte, la transmisión, la velocidad intraxónica y la acción farmacológica.
Si bien el mayor sustrato para la formación de serotonina es el triptófano, el colesterol también participa como agente precursor. De esta forma la disminución del colesterol disminuye el sustrato para serotonina, y su producción somatoaxónica.
La disminución del colesterol estaría implicado en el aumento de la recaptura presináptica. De esta forma habría una relación entre colesterol, receptor presináptico y aumento de la inhibición de liberación de serotonina. Las bajas tasas del colesterol son homologables a un descenso de la capacidad del organismo de generar receptores postmembrana. Por consiguiente un descenso del colesterol tendría una disminución de la respuesta global a los psicofármacos, por ejemplo un efecto anti IRSS.
Se pudo constatar que los efectos antiimpulsivos de la carbamazepina, en la segunda semana de tratamiento, dependen también del aumento de colesterol total que produce la carbamazepina. Esta elevación de los niveles de colesterol total, se acompañan en su acción antimpulsiva y anticonvulsiva de la activación de los receptores GABA periféricos. Este aumento del transporte del colesterol intramitocondrial (por acción del GABA y de la carbamazepina) convierten el colesterol intramitocondrial en pregnenolona; que se transforma en neuroesteroides específicos como son el 3-alfahidroxi-5-A-pregno-20-ona y el 3-alfa-21dihidroxi-5-A-pregno-20-ona. Estos neuroesteroides conjuntamente con el aumento del colesterol, serían los responsables de los efectos antiagresivo y anticonvulsivo de la carbamazepina (cap. 2).
Por consiguiente los fármacos hipocolesterinizantes, como los usados en la actualidad -potentes y rápidos en lograr el descenso del colesterol- deberán ser utilizados con precaución en los pacientes que presenten historia de riesgo suicida, impulsividad y/o violencia (35).
En un estudio que hemos realizado en 30 pacientes sobre las conductas violento-impulsivas y su relación con el colesterol, sólo un 33 % presentó niveles normales o altos de colesterol siendo en su mayoría mujeres.
Por ello es aconsejable que el descenso de los niveles de colesterol se realice bajo vigilancia médica en:
1) Pacientes depresivos, con riesgo suicida y en esquizofrenia de tipo II dado su hipocoloesterolemia.
2) Pacientes hipocolesterinémicos, medicados con clozapina por la posibilidad de la disminución de su actividad terapéutica, ya que podría la clozapina no fijarse, al disminuir la cantidad de receptores específicos a la serotonina.
3) Pacientes con psicosis y agitación psicomotriz, ya que se observó que tanto ellos, como sus familias, registran antecedentes con elevación del colesterol, prolactina y viscosidad de membrana.
4) Pacientes violentos bajo tratamiento con carbamazepina, por la capacidad
de la misma de reducir el colesterol total.
1-27. Glosario de términos y abreviaturas en psiconeurobiología
La mayoría de los términos son originarios del inglés, se expresan en forma original, única forma de respetar su sentido. En general la nomenclatura científica nóvel, si bien admite traducción, aparece en castellano, luego de un período de uso y estudio.
Actividad N-metilante
La actividad metilante en sangre total (actividad N-metiltransferasa, ANMT) es un procedimiento de utilidad para determinar su incremento. Un aumento puede indicar alta vulnerabilidad clínica en comparación con pacientes que no la poseen. Hemos observado en pacientes esquizofrénicos y borderlines que dicho aumento se asocia, ante situaciones estresantes, a recrudecimiento de la patología psicótica (inclusive la aparición de actividad alucinolítica y delirante de comienzo abrupto).
Adenilciclasa
Enzima capaz de catalizar la formación del AMP cíclico. El AMP cíclico es uno de los segundos mensajeros más importantes y tiene la capacidad de hacer reaccionar el complejo de proteinoquinasas. Este proceso de activación se puede dar en múltiples lugares en lo que respecta a la información biomolecular (factores de transcripción, enzimas, receptores proteicos, información nuclear, etc).
Agonista
Es la estimulación de un receptor por un ligando. Luego de esta acción continúan una serie de reacciones, que comienza con la activación de la proteína G, la unidad catalítica y los segundos mensajeros.
Agonista inverso
Provoca la acción opuesta al agonista. No bloquea al agonista desde la apertura del canal, como lo hace un antagonista. Sin embargo la más clara diferencia con un antagonista es que el agonista inverso nunca abre los canales iónicos sino, por el contrario, produce su cierre. Por otra parte un antagonista puede actuar sobre un agonista inverso, tal cual lo hace sobre un agonista.
Agonista parcial
Ejerce un efecto similar al agonista completo, pero su acción sobre el receptor es más débil. El agonista parcial también es bloqueado por los antagonistas, de la misma forma que un agonista inverso también puede ser parcial.
Antagonista
Es el bloqueo de la acción de todo tipo de agonistas. Por sí mismo un antagonista no tiene actividad. Es necesaria la presencia de un agonista para que el antagonista bloquee su acción.
Apoptosis
Es un programa de muerte celular, regulado genéticamente, caracterizado por la condensación de la cromatina y la fragmentación en varios puntos del ADN por una endonucleasa. Se forman vesículas apoptósicas celulares que finalmente son fagocitadas. En la actualidad existe un acuerdo que, cuando se habla de apoptosis, se hace referencia a la muerte celular como producto del proceso degenerativo de las proteínas TAU, por factores de la modificación de la proteína G120-macrófago, que produce fagocitación celular aberrante.
BTLE
El Brief Temporal Lobe Epilepsy es una sigla para describir un síndrome característico de pacientes que presentan pequeños signos epileptiformes, que se propagan con una máxima intensidad, pero en una mínima expresión de tiempo. Esto explicaría las reacciones de furia espontánea -con una fuerte descarga de violencia-, con un rápido regreso a la calma, que este tipo de pacientes presentan frente a un suceso leve o moderadamente frustrante. Ocurre con mayor frecuencia en pacientes con trastorno límite o borderline de la personalidad.
BRR
Es la sigla conocida del Brain Reguard Region. Se podría decir que es el centro cerebral de la recompensa. Es el área donde además de otros estímulos, provocan sus efectos drogas como la cocaína, anfetaminas, crack, etc.
BTC
Es la sigla conocida del Brain Trauma Center (centro de trauma cerebral). Es un triángulo estratégico de función neuroanatómica que regula los procesos de ansiedad crónica y del estrés postraumático. Está formado por tres subestructuras: el eje hipotálamo-hipófiso-adrenal, la amígdala y el locus coeruleus.
Blue print
Es el anteproyecto celular contenido en el ADN. Conlleva toda la carga genética e incluye desde las formas mínimas de vida hasta el ser humano. Es el polo nuclear de la información celular y la modificación del mismo podría tener efectos milagrosos o dramáticos, dependiendo si sobre él actúa un estimulo beneficioso o uno nocivo.
cis
Son sitios de ligadura que pueden ser encontrados en los genes. Los cis si bien participan del proceso de transcripción, pueden también comportarse como elementos represores y verificadores de la señal recibida.
c-fos/c-jun
Si bien son protooncogenes, que participan en el proceso de transcripción, también se comportan como proteínas represoras. Tienen la propiedad de lectura del mensaje. Pueden aceptar o reprimir la información. El c-fos y el c-jun pueden modificarse en condiciones experimentales en animales de laboratorio sometidos a estrés crónico, También se puede modificar en pacientes con trastornos por estrés postraumático.
Se lo llamó jun como abreviatura de junana (17 en japonés) por ser el 17 en un grupo de 30 virus de sarcomas de aves.
El c-fos se expresa rápidamente como respuesta a los factores de crecimiento. Codifica una fosfoproteína que funcionaría como mensajero en el proceso de transducción. Se lo llamó así por ocupar un lugar, luego de los osteorsarcomas llamados FBJ y FBR.
Comunicación bidireccional
Con este término se denominan dos procesos de interacción:
1) El estudio de la interrelación mente-cerebro-estímulo. Su objeto de estudio es la repercusión de la biología en el proceso de pensamiento y emoción por un lado, y la acción del proceso mental y del medio ambiental sobre el estado biológico y estructural del cerebro, por el otro. Las áreas de investigación son: apoptosis, citoarquitectura, estratificación y reconocimiento de diferentes circuitos relacionados con trastornos psiquiátricos.
2) El estudio de comunicación bidireccional como el proceso de interacción entre el sistema inmunológico y el sistema nervioso central. Este proceso es el objeto de estudio de la psico-bio-inmuno-oncología.
Cross talk
Se llama así a dos tipo de procesos:
1) Al proceso de retroalimentación o feedback entre los segundos mensajeros, el receptor y la señal primaria, también conocido como proceso de feedback vertical.
2) Al proceso de interacción horizontal entre dos señales primarias que actúan en forma de feedback horizontal entre diferentes señales que llegan a diferentes receptores.
Se podría decir que el cross talk es un descubrimiento reciente, que informa acerca de la comunicación cruzada que existe entre dos señales primarias que llegan a dos receptores diferentes. Antes se pensaba que los caminos de comunicación eran sólo verticales en dirección de adentro-afuera o de arriba-abajo. Hoy se conoce que existe una comunicación de afuera hacia adentro, de abajo hacia arriba y entrecruce de información entre las diferentes líneas del information flow. Esto hace pensar que los receptores no funcionan aisladamente sino, por el contrario, lo que le ocurra a un receptor afectará a su receptor vecino.
Espectro
El concepto de espectro se aplica al grupo de subtrastornos que podrían tener un deterioro neurobiológico de similar explicación. Así, por ejemplo, si se encontrase una disfunción en un sistema neurobiológico, se podría decir que tal disfuncionalidad no es específica de un trastorno, sino del espectro de dicho trastorno. Un ejemplo de esto son los estudios neurobiológicos sobre esquizofrenia, que no se encuentran en tal o cual tipo de esquizofrenia, sino en el espectro esquizofrénico. Otro ejemplo es el espectro obsesivo: las investigaciones neurobiológicas sobre la disfuncionalidad del cíngulo, podrían servir para explicar parcialmente al espectro obsesivo, y no específicamente a un tipo especial de trastorno obsesivo.
Factores de transcripción
Son proteínas complejas encargadas de activar la secuencia del promotor del gen, para que actúe la ARN-polimerasa 11, que inicia la transcripción del ARNm. Los factores de trascripción basales más conocidos son el TFIID, TFIIA, TFIIB, etc. El TFFID es una proteína presente en casi todas las células, ya que está unido a la TATA box (TBP: TATA binding protein; y a la TAF.- TBP associated factor), que al alterar la forma rectilínea de la cromatina del promotor y curvarla a 100′ permite la duplicación, a través de la polimerasa 11 del ADN y el comienzo de la transcripción del ARNm.
Factores de crecimiento
Es un grupo de citoquinas que tienen la capacidad de estimular el crecimiento y proliferación celular (factor de creciminto epidérmico, factor neurotrófico cerebral (BDNF, brain derived neurotophic factor), etc.
Full blown
Golpe reiterado o repetido. El concepto neurobiológico que lo define es un microestímulo con capacidad de producir modificación de la memoria celular, que puede ser tanto en fase aguda como crónica.
HPA
Con esta sigla se conoce al eje hipotálamo-pituitario-adrenal. Es el eje más estudiado en los desórdenes producidos por estrés. La activación de este eje en los pacientes con vulnerabilidad psicótica, puede producir un aumento del volumen de actividad N-metilante sobre la suprarrenal, desencadenando procesos psicóticos.
Interleuquinas
Se llama así a un conjunto de factores proteicos producidos por macrófagos y linfocitos T. Existen diferentes tipos de interleuquinas: interleuquina I (IL-1), dividida en dos subtipos, las tipo alfa y las tipo beta. Es producida por macrófagos que inducen la proliferación de otro tipo de interleuquina, llamada interleuquina 2 (IL-2). La vía de producción que utiliza son los linfocitos. Se pueden también denominar por la sigla que indica su acción. Así la IL-1, como otras interleuquinas, es conocida como LAF (Factor activador de linfocitos), y está relacionada con los procesos inflamatorios.
La interleuquina 2 (IL-2) proviene de la IL-1; para su activación es necesaria una activación de antígeno o nitrógeno. Está relacionada con el factor de crecimiento de los linfocitos T y con la producción de interferón. Tiene una acción antitumoral para tumores sólidos.
La interleuquina 3 (IL-3) es el factor estimulador principal de las células madre de la médula ósea. Activa el proceso de diferenciación celular para células eritropoiéticas, mastocitos, granulocitos y macrófagos.
A nivel neurobiológico, forman parte de lo que se conoce como el estudio de la comunicación bidireccional.
Las acciones de las interleuquinas están asociadas a diversos factores como son: interacciones psicofarmacológicas con antidepresivos, interacciones neuroinmunobiológicas (vía inmunoneuropéptidos), reacciones de inhibición en la depresión (duelo, estrés), liberación de la hormona liberadora de corticotrofina (CRH) por activación de la interleuquina-6 (IL-6), inhibición y/o estimulación en las diferentes fases del proceso de la esquizofrenia, relación de las interacciones psicofarmacológicas, acción sobre factores de crecimiento tumoral o factores de necrosis tumoral, etc.
Kindling
Activación de tipo espontánea (convulsiones), producida por una descarga total, provocada, luego de reforzamientos continuos subliminales (que no causaban convulsiones). El kindling puede ser inhibido por los barbitúricos, las benzodiazepinas y desencadenado por estímulos como el alcohol, la cocaína, la anfetamina, etcétera.
Long lasting sensitization, Long Term Potentiation
El proceso de sensitization, si bien puede producir cambios estructurales en los receptores, en general está más referido a las modificaciones cuantitativas y no a las cualitativas.
El long lasting, en cambio, está referido a factores cualitativos, en los cuales pueden actuar elementos de transcripción [C-fos, C-jung o los activados por factores de stress o crecimiento: (Grb 2, Ras, Raf Kinasa, » Kinasa, etc)].
En este caso ya existen modificaciones estructurales de la expresión genética y remodelamiento microestructural. Un ejemplo de esto sería cuando el estrés incontrolable produce potenciación a largo plazo (Long term potentation), sobre regiones de alarma cerebral como son el locus coeruleus y la amígdala. En este caso se produce una consolidación de memoria neurobiológica. También son los cambios que se producen por un adecuado tipo de respuesta farmacológica (tipo IV Responde y Aprende, RA).
MEF
Es la sigla conocida para el área medial-estriatal-frontaL Esta área esta involucrada en los procesos de formación del tono celular. Está regulada por las células CAI, piramidales-dopa-hipocampal. También está relacionada con el déficit cognitivo en las esquizofrenias tipo II.
Pérdida celular
Se refiere a la pérdida de la función celular producida por el full blown. El caso típico es la pérdida de las funciones específicas de las neuronas de diferentes áreas del cerebro en pacientes con el trastorno por estrés postraumático.
PIP2
El PIP 2 es el fosfatidilinositol 4,5-bifosfato, presente en la membrana celular, que es hidrolizado por una fosfolipasa C, que es el factor que inicia la propagación y producción de segundos mensajeros: inositol 1,4,5-trifosfato (IP-3) y el diacilglicerol (DAG). Con la formación de un grupo de ATP, se forma el fosfatidilinositol 4-fosfato, que se origina del fosfatidil-inositol por la catalización de una proteinoquinasa, va a generar, luego de algunos pasos intermedios, la fosfolipasa CB.
Proteína G
Es una proteína de membrana subdividida en unidades alfa, beta y gama; a su vez cada una de ellas se vuelven a subdividir en otras subunidades. La activación de la proteína G, a través de ligaduras de fosfatos, produce la ruptura de esta unión de las subunidades. Su separación funcional permite que los ligandos atraviesen la membrana celular. Pertenece a la familia de los nucleótidos de guanina. Existen diferentes tipos de proteínas G: activadoras e inhibidoras. Todas ellas regulan procesos de señales intracelulares inhibiendo, estimulando u organizando la señal. Actúan en la unidad catalítica sobre los fenómenos de fosforilación hacia los segundos y terceros mensajeros.
Proteínas represoras
Es un conjunto de proteínas y sistemas que verifican cuál es el tipo de señal recibida. Actúan como una aduana nuclear protectora del blueprint. Estas proteínas pueden ser engañadas por algunos estímulos nocivos.
Proteinoquinasas (PK)
Son enzimas intracelulares, codificadas en los cromosomas 16, 17 y 19. Intervienen en numerosos procesos celulares: transducción y secreción hormonal. Pueden ser activadas por señales extracelulares y activar segundos mensajeros como son el DAG y el IP-3, movilizando los depósitos cálcicos.
Protoncogenes
Son genes que codifican proteínas, que controlan la proliferación celular. Codifican numerosas proteínas importantes como son por ejemplo los factores de crecimiento, proteínas nucleares que actúan como factores de transcripción (Fos, Jun), el receptor para la hormona tiroidea, situado en el citosol, etc.
Cuando los protoncogenes se transcriben de manera aberrante se convierten en oncogenes (muchos virus son portadores de oncogenes).
Sensitization
Se refiere al aumento de la susceptibilidad de membrana y de todos los organismos que la componen: receptores, canales iónicos, receptores mixtos, unidades catalíticas, proteína G, proceso de fosforilación, etc. Forma parte del proceso de neurovulnerabilidad general y es el paso previo obligado para la vulnerabilidad de membrana. Los receptores pueden cambiar su velocidad de transducción, su número o densidad y su arquitectura. Es indispensable que se desarrolle el proceso de sensitization antes del conocido long lasting sensitization. Este proceso está relacionado con la estimulación transitoria. Es el caso del sujeto no adicto que consume durante un tiempo no prolongado cocaína o anfetaminas, que si bien produce una modificación de los receptores, el escaso tiempo (el escaso full blown) no alcanza a producir long lasting sensitization.
Pruning
Poda de brotes dendríticos aberrantes, que aparece desde los primeros momentos de la vida y que evita el proceso de sinapsis redundantes.
TATA Box
La TATA box es una caja de nucleótidos de tipo adenina y timina, de allí su nombre: T-A-T-A, que se encuentran 25-35 bases abajo del sitio de transcripción y a través de los factores de transcripción y las polimerasas 1 y 11 participan o son responsables de la transcripción genética.
Tono celular
El tono celular es el estado de una neurona en su capacidad de respuesta al medio. Se supone en la actualidad que existe un tono celular normal o débil celular para el sujeto no violento y un tono celular hipersensible para el sujeto con extraversión y violencia. En la regulación del tono celular participan la serotonina y el colesterol.